originale
Studiul reacțiilor adverse legate de perfuzia Paclitaxel și Docetaxel
Studiu privind Reacții de publicitate legate de paclitaxel și perfuzie docetaxel
i. J. Castro1, M. Pons Buom1, GI Ballesteros Cabañas1, E. Ramió Montero1, A. Álvarez Méndez2, R. De Castro Chivato3, M. Centelles Ruiz4
1service de farmacie, Spitalul Capio Universitari Sagrat CoR, Barcelona, Spania.
Serviciul de Farmacie 2Nfermera, Spitalul Capio Universitari Sagrat Cor, Barcelona, Spania.
Spitalul de Zi 3enrmEra, Spitalul Capio Universitari Sagrat Cor, Barcelona, Spania.
4Songologie, Spitalul Capio Universitari Sagrat Cor, Barcelona, Spania.
Această lucrare a fost parțial prezentată ca o comunicare poster în cel de-al 56-lea Congres Național al Societății de Farmacie spaniolă care a avut loc la Santiago de Compostela De la 18 la 21 octombrie 2011.
Management pentru corespondență
Rezumat
Obiectiv: Pentru a determina incidența reacțiilor la perfuzia de paclitaxel și docetaxel și Cauzele posibile care le pot declanșa.
Metoda: Studiul CohorT al Paclitaxel Infuzii și Docetaxel efectuate la un spital al treilea nivel, din iulie 2010 până în decembrie 2011 (18 luni). Pentru fiecare perfuzie, datele clinice ale pacientului și cele referitoare la taxanul gestionat au fost înregistrate. Având în vedere apariția unei reacții în timpul perfuziei, a fost specificată: tip, severitate și dacă a forțat suspendarea tratamentului. Au fost consultate povestiri clinice și ordine medicale. Urmărirea perfuzilor a fost efectuată prin contactarea asistenților medicali de zi. Un studiu descriptiv al celor mai relevante variabilele incluse în urma ulterioară a fost efectuată și analizată dacă oricare dintre ele ar putea influența apariția reacțiilor.
Rezultate: În timpul perioadei de studiu, au fost administrate 357 de perfuzii de paclitaxel și docetaxel la 92 de pacienți: vârsta medie de 61,4 ani (de la 11,1), 50,0% femei. Au fost detectate 9 reacții infuresonale care au afectat 8 pacienți, toate cauzate de docetaxel (χ2 = 8,3, p = 0,004); 14,5% dintre pacienții care l-au luat și întotdeauna în timpul primului sau al doilea ciclu de tratament. Variabilele asociate semnificativ cu apariția reacțiilor au fost: neoplasm pulmonar (p < 0.005), schemă docetaxel-cisplatină (p < 0.005) , Primiți medicamentul pe prima linie (p = 0,021) și boala fără cunoaștere (p = 0,014).
Concluzii: În centrul nostru de spital, Docetaxel este taxanul care a provocat mai multe probleme de securitate în timpul perfuziei dvs.
Cuvinte cheie: paclitaxel; Docetaxel; Reacția de hipersensibilitate.
Rezumat
Obiectiv: Pentru a determina incidența reacțiilor asociate perfuziei paclitaxelului și docetaxel și cauzele probabile care le pot declanșa.
Metoda: Studiul cohortei a perfuzilor Paclitaxel și Docetaxel efectuate la un spital terțiar din iulie 2010 până în decembrie 2011 (18 luni). Pentru fiecare perfuzie, au fost înregistrate datele clinice și datele legate de droguri. Când a apărut o reacție în timpul perfuziei, au fost specificate următoarele date: tip, severitate, dacă a fost necesară retragerea tratamentului. S-au revizuit diagramele clinice și comenzile de tratament. Urmărirea perfuzilor a fost făcută prin contactarea asistenților spitalici de zi. S-a făcut un studiu descriptiv pentru cele mai relevante variabile incluse în urmărirea și am analizat dacă oricare dintre ele ar fi putut avea o influență asupra apariției reacțiilor.
Rezultate: În timpul perioadei de studiu, 357 de perfuzii Paclitaxel și Docetaxel au fost administrate la 92 de locuri: vârsta medie de 61,4 ani (SD 11.1), 50,0% au fost femei. 9 reacții cu perfuzie care afectează 8 ani, toate cauzate de docetaxel (χ2 = 8,3, p = 0,004); 14,5% dintre pacienții o recuperează și întotdeauna în timpul primului sau al doilea ciclu de tratament. Variabilele asociate semnificativ la apariția reacției: cancer pulmonar (p < 0,005), regim de docetaxel-cisplatină (p < 0.005) , Primind medicamentul ca primă linie (p = 0,021) și boala non-avansată (p = 0,014).
Colabile: La spitalul nostru, Docetaxel este taxanul care a provocat cele mai frecvente probleme de siguranță în timpul perfuziei.
Cuvinte cheie: paclitaxel; Docetaxel; Reacția de hipersensibilitate.
Introducere
De la câteva decenii în urmă, pachetele de taxe și docetaxel s-au dovedit a fi eficiente într-o varietate de tumori. Paclitaxelul este aprobat pentru tratamentul sânilor, celulelor mici (celule mici) și neoplasmelor ovariene; și docetaxel pentru sân, pulmonar (celule non-mici), cap și gât, adenocarcinom gastric și prostată1,2.Acțiunea citotoxică a Taxanului este susținută în stabilizarea tubulinei și formarea ulterioară a microtubulilor nefuncționali care declanșează o mitoză eronată, astfel încât celulele canceroase să nu mai împărțiți și s-au încheiat cu moarte1-3. În studiile preclinice, docetaxelul sa dovedit a fi mai eficace decât paclitaxelul, deoarece se alătură tubulin cu afinitate mai mare, prezintă o acțiune antitumorală directă prin activarea căilor apoptotice și o retenție mai mare în celulele tumorale4.
Unul dintre dezavantajele prezentate Prin aceste substanțe este solubilizarea lor slabă, prin urmare necesită utilizarea vehiculelor de surfactant neionic pentru formularea lor. Cremofor, derivatul polioxietilat al uleiului de ricin, este solubilizarea utilizată pentru paclitaxel și polisorbat 80 (Tween 80), un alt derivat polioxietilat, este pentru docetaxel. Aceste două vehicule cresc interacțiunile farmacologice cu alte antineoplastice (de exemplu, antharaclinele) și pot modifica farmacocinetica medicamentelor cu care sunt formulate, predispuse la o toxicitate mai mare, în special în cazul paclitaxelului prin farmacocinetica non-liniară4-6. Pentru a minimiza reacțiile adverse, evitați premedicarea și scăderea timpilor de administrare paclitaxel și docetaxel, au fost dezvoltate noi strategii de formulare, cum ar fi nanoparticule de albumină, polignatamați, promedicamente, emulsii sau lipozomi5. Până în prezent, numai noua formulă Paclitaxel bazată pe nanoparticulele de albumină (Abraxane®) a fost comercializată în Spania.
Profilul de siguranță al acestor agenți antitumorali este divergent; În timp ce paclitaxelul este mai asociat cu neuropatiile periferice, mialgii și arthralgii, Docetaxel se află la reținerea lichidelor (creșterea în greutate, inflamația gleznelor sau zonei abdominale) 5.7. Aproximativ cu aceeași frecvență, cele două medicamente pot provoca reacții la perfuzie (dispnee, durere toracică, angioedem, urticarie, urticarie și erupție cutanată) care depind de caracteristicile taxanului, solventului sau ambelor și ale căror apariții este posibilă , printre alte cauze, la perfuzia rapidă a acestor preparate8,9. Aceste reacții, adesea numite și reacții de hipersensibilitate, apar de obicei în primele minute ale perfuziei și, în general, în prima sau a doua doză, fiind capabili să apară chiar și cu premedicarea adecvată pe bază de corticosteroizi și antihistaminice8.10.
Toate Acest lucru ne-a motivat interesul față de determinarea incidenței reacțiilor adverse legate de perfuzarea Paclitaxelului Taxs și Docetaxel în centrul nostru, și cauzele posibile care le pot declanșa.
Metoda
Observațional, longitudinal și potențial studiu al tuturor infuziunilor Paclitaxel sau Docetaxel din iulie 2010 până în decembrie 2011, într-un spital universitar de nivel 3 fără transplanturi.
Pacienții tratați cu paclitaxel au primit premedică orală cu dexametazonă 8 mg cu o zi anterioară la chimioterapie și în aceeași zi intravenos: ondansestron 8 mg, dexameton 8-12 mg, dexclorofeniramină 5 mg și ranitidină 50 mg, 30 minut OS înainte de administrarea dvs. Premedicația utilizată pentru docetaxel a constat din dexametazona orală de 8 mg de două ori pe zi timp de trei zile, începând cu o zi înainte de chimioterapie, și, de asemenea, în aceeași zi intravenos: ondansestron 8 mg și dexametazonă 8-12 mg, cu 30 de minute înainte de administrare.
Mărcile utilizate au fost Paclitaxel Hospira® în cazul Paclitaxel și Taxotere® și Docetaxel Hospira® pentru Docetaxel. Docetaxelul a fost administrat în ser fiziologic de 250 ml timp de 60 de minute și paclitaxel în serul fiziologic de 500 ml în 180 de minute de perfuzie. În poliquiimioterapie, taxanele au fost întotdeauna administrate mai întâi, astfel încât reacțiile care ar putea apărea în primele minute ale perfuziei nu le pot fi atribuite numai.
O urmărire zilnică a fost efectuată din toate administrațiile de taxani și Au fost înregistrate următoarele variabile:
divid id = „1CA402628F”>
• Date despre pacient: vârstă, sex, număr de istoric clinic și oncolog responsabil.
• clinică Date: Neoplazia, stadionul, istoria patologică, alergiile, medicamentele obișnuite și tratamentele chimioterapeutice anterioare în cazul în care au fost.
• Date privind tratamentul oncologic: Tipul de taxan (inclusiv numele comercial), doza, frecvența, ciclul, concomitent chimioterapie și premedicație.
• Aspectul oricărei reacții adverse (RAM) în timpul perfuziei de taxan, specificarea tipului și severității în conformitate cu clasificarea NCI-CTCAE V.3.0 2006 a insuficienței cancerului național11 .
Pentru a înregistra datele referitoare la pacient, au fost consultate înregistrările medicale.Datele referitoare la tratamentul oncologic au fost obținute din prescripție medicală de către pacientul și ciclul de tratament. Urmărirea fiecărei perfuzii a fost efectuată de farmacistul responsabil pentru domeniul citostaticilor și farmacistului rezident prin contactarea asistentei medicale a spitalelor responsabile de administrarea taxanului. Raportul de cauzalitate a reacțiilor a fost determinat de algoritmul Karch-Lasagna modificat12.
Analiza statistică a variabilelor calitative și cantitative a fost efectuată cu programul SPSS V.15.0. Sa evaluat dacă variabila dihotomă principală nu este asociată semnificativ cu fiecare dintre variabilele independente. Testul Chi-pătrat a fost utilizat pentru variabilele categorice și elevul T pentru compararea mijloacelor în eșantioane independente, luând p < 0,05 ca raport statistic semnificativ.
Studiul a fost aprobat de Comitetul de etică al cercetării clinice spitalicești și este necesar pentru punerea în aplicare a firmei de consimțământ informat de către pacienții care au îndeplinit criteriile de includere.
Rezultate
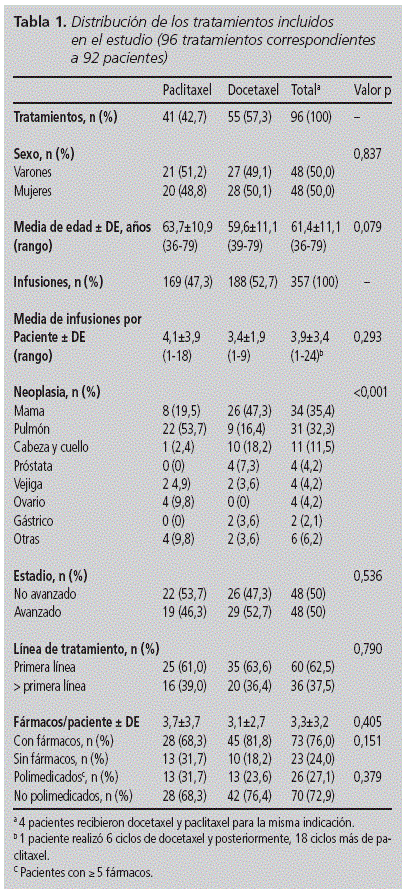
În timpul celor 18 luni de studiu , 4,689 de medicamente oncologice au fost infuzate, dintre care 7,6% au corespuns taxanilor incluși în urma ulterioară. În total 357 de perfuzii de paclitaxel și docetaxel administrate la 92 de pacienți (50,0% femei), cu vârsta cuprinsă între 36 și 79 și o vârstă medie de 61,4 ani (de la 11.1). Docetaxel a fost cel mai frecvent utilizat taxan în număr de pacienți (n = 55, 57,3%) și perfuzii (n = 188, 52,7%). Nu s-au constatat diferențe semnificative în variabilele bazale ale ambelor cohorte, cu excepția distribuției neoplasmelor (tabelul 1): cea mai frecventă indicație pentru docetaxel a fost cancerul de sân (47,3%), în timp ce pentru paclitaxel a fost pulmonarul (53,7%). Mai mult de jumătate dintre pacienți au primit tratamentul pe prima linie (62,5%).
A fost folosit un total de 36 Protocoalele chimioterapeutice, fiind cea mai utilizată schemă atât pentru docetaxel, cât și pentru paclitaxel, combinația cu carboplatină (cap și gât și, respectiv, cancerul pulmonar) (tabelul 2).
9 reacții infuresonale care corespund la 8 pacienți (8,7% din Totalul), toate cauzate de docetaxel (χ2 = 8,3, p = 0,004) și întotdeauna în timpul primului sau al doilea ciclu de tratament. Astfel, 4,8% din perfuzii docetaxel au cauzat o reacție, dintre care 66,7% (n = 6) au apărut în al doilea ciclu de tratament și au ajuns să afecteze 14,5% dintre pacienții care au primit această chimioterapie. Dacă sunt selectate numai perfuzele Docetaxel administrate în timpul primului sau al doilea ciclu, incidența reacțiilor crește până la 10,5% din administrație. În toate cazurile, reacțiile au apărut la pacienții cu vârsta mai mică de 65 de ani (56,3 ani), nu polimedicată, fără a se cunoaște alergii anterioare și pe prima linie de tratament.
66,7% ( n = 6) a reacțiilor au fost considerate moderate în conformitate cu NCI-CTCAE V.3.011. Într-unul din cazuri, reacția a fost considerată foarte gravă, deoarece au fost necesare măsuri de sprijin vitale. Acesta a fost singurul caz în care reacția a motivat suspendarea tratamentului. La 6 pacienți, retragerea docetaxelului a fost tolerată fără probleme, iar la doi pacienți au fost administrați ulterior paclitaxel fără incident (Tabelul 3). Conform algoritmului de la Karl-Lasagna modificat12, toate reacțiile au fost clasificate ca probabile.
în grupul de bărbați 5 reacții au apărut ca un cancer pulmonar comun de numitor și schemă Docetaxel 75 mg / m2 + cisplatină 75mg / m2 c / 21 de zile. Această schemă a fost administrată la un total de 6 pacienți, astfel încât 83,3% dintre cei care au primit acest protocol au prezentat o reacție la perfuzie. În cele 3 reacții care au apărut la femei, singurul neoplasm implicat a fost sânul, iar protocoalele chimioterapeutice au fost de 2 ori combinația cu trastuzumab și într-una cu carboplatină.
în acest studiu variabilele care sunt corelate Statistic cu apariția reacțiilor la perfuzia Docetaxel a fost: neoplasm pulmonar (p < 0.005) , primiți medicamentul pe prima linie (p = 0,021) și în boala non-avansată (p = 0,014). Cu toate acestea, o astfel de corelație nu a fost observată cu variabilele sexuale, de vârstă și de medicamente obișnuite.
Discuție
Eficacitatea taxanelor poate fi compromisă prin apariția reacțiilor de hipersensibilitate în timpul perfuziei sale. Uneori, acestea pot forța să suspende tratamentul care trebuie să recurgă la alte sisteme care ar putea fi mai puțin eficiente.
În literatura științifică este descris faptul că docetaxel și paclitaxel provoacă reacții de hipersensibilitate cu o frecvență aproape de 30%, dar scade până la 2-5% dacă pre-tratamentul se efectuează cu corticosteroizi și antihistaminice și dacă este a redus rata de perfuzie1,2,8,13,14. În studiul nostru, paclitaxelul nu a provocat nicio reacție cu premedicarea folosită și infuzată pentru 3 ore2. Cu toate acestea, 9 episoade au apărut cu docetaxel (14,5% dintre pacienți), administrându-l timp de o oră și experți la spitalul de zi premedicarea recomandată pe siguranța tehnică1. Cele mai multe reacții (6) au fost rezolvate prin consolidarea premedicației și reducând viteza de administrare de 250 ml / h la 125 ml / h și crește ulterior viteza progresivă. Unii autori, în afară de reducerea vitezei de administrare, recomandă, de asemenea, alte opțiuni, cum ar fi reducerea concentrației de medicament care urmează să fie administrată sau luând în considerare aplicarea protocoalelor de desensibilizare prin creșterea perfuzilor de doze15. Există studii care susțin, de asemenea, schimbarea unui taxan prin altul atunci când o reacție de hipersensibilitate apare la una dintre ele19-21. Desigur, schimbarea reciprocă poate favoriza continuarea tratamentului, totuși există controverse în această privință, deoarece alți autori, cum ar fi Dizon et alții, consideră că acest lucru nu este posibil din cauza existenței unei reactivități transversale între taxani. În urmărirea noastră nu a existat nici o reactivitate încrucișată, deoarece doi pacienți care au prezentat o reacție infuzională la docetaxel au primit paclitaxel fără incident. La 6 pacienți, retragerea Docetaxel a fost bine tolerată, însă a existat un pacient care, după prezentarea unei reacții moderate la docetaxel, re-primirea acestui taxan și a prezentat din nou o reacție, de această dată considerată severă și care a cauzat suspendarea definitivă a tratamentului. În orice caz, ceea ce este clar este că administrarea oricărui taxan este contraindicată dacă reacția de hipersensibilitate cauzată de oricare dintre ele este severă (gradul 3-4) 1.2.
simptome legate de aceste reacții, de obicei apar în prima sau a doua perfuzie de chimioterapie și, în general, în câteva minute de pornire, așa cum sa întâmplat la cei 9 pacienți afectați în urmărirea noastră. Prin urmare, o atenție specială trebuie plătită în primele administrații de taxane, organizând în orice moment personalului experimentat și sprijinul unei echipe de resuscitare în cazul în care a existat o reacție care amenință viața pacientului22. Altă îngrijire care ar putea fi efectuată sunt monitorizarea tensiunii arteriale și observarea pacientului până la 2 ore după administrarea taxanului.
În studiul nostru, simptomatologia pacientului care a avut o reacție infuzională la docetaxel Foarte gravă a fost caracterizată de cianoză , pierderea conștiinței, criza, insuficiența respiratorie și hipotensiunea. Imaginea a fost inversată rapid după oprirea perfuziei și cu ajutorul corticosteroizilor, terapiei de oxigen și flidoterapie; Această reacție a fost notificată la centrul regional de farmacovigilență. În celelalte cazuri cele mai mici, reacțiile au constat din eritem cutanată, roșie facială, durere lombară, tahicardie și, în unele cazuri, frisoane, hipotensiune și amețeli. În nici unul dintre ele nu au existat dispnee sau bronhospasm. Nu există nicio îndoială, care să reducă riscul apariției acestor evenimente este de a crește pacienții din prepararea adecvată a premedicărilor care sunt plătite. Administrarea unui premedicație bazată pe antihistaminice și corticosteroizi înainte de taxan este de alegere, deoarece sa demonstrat că reduce incidența și severitatea retenției de fluid, precum și severitatea reacțiilor de hipersensibilitate1,2,7. În plus, evită întreruperile în tratament și permite creșterea dozelor cumulative ale taxanelor8.
Nu se cunoaște dacă aceste reacții depind de solvent sau de taxan sau de ambele componente. Nici mecanismul pentru care apar. Se crede că acestea pot fi mediate de activarea complementului, eliberarea nespecifică a histaminei, producția de oxid nitric sau prin eliberarea citokinelor. Contrar a ceea ce se întâmplă cu derivații de platină, în principiu nu se referă la aspectul său cu un mecanism mediate de IgE, deoarece reacțiile apar de obicei în câteva minute de pornire a perfuziei în timpul primului sau al doilea ciclu de tratament, ceea ce sugerează că nu este nevoie pentru pre-sensibilizare23-25.Un alt aspect care trebuie luat în considerare și că, cu bibliografia consultată, nu a fost elucidată cu acuratețea8,26, este de a determina dacă există aspecte clinice sau subiective care ar putea predispune pacientului la o reacție de hipersensibilitate acută sau la orice alt memoriu berbec.
În studiul nostru, factorii care au fost strâns legați de apariția reacțiilor infuzionale au fost: neoplazia pulmonară, schema de docetaxelcisplatină, primește medicamentul pe prima linie și fără probleme. Dintre acești factori, în literatura de specialitate, consultată numai pentru a primi docetaxel în prima sau a doua linie a fost considerată o variabilă decisivă în apariția acestor reacții.
Pe de altă parte, este posibil ca concomitent Utilizarea paclitaxelului sau docetaxel cu alți antineoplastici, cum ar fi trastuzumab, carboplatină sau cisplatină, poate spori apariția reacțiilor de hipersensibilitate, deoarece ei înșiși pot, de asemenea, să le provină. Trastuzumab, ca și taxanele, determină de obicei aceste reacții în primul sau al doilea ciclu, dar acestea nu sunt prezentate în câteva secunde de pornire a perfuziei27. În schimb, reacțiile derivatelor de platină apar în cea mai mare parte din cel de-al șaselea ciclu, în timpul sau mai târziu la perfuzia lor25,28. În studiul nostru, toate reacțiile au apărut la pacienții cu tratament polimetiotic cu aceste medicamente: 6 în combinație cu cisplatină, 2 cu carboplatină și 1 cu Trastuzumab. Cu toate acestea, numai relația poate fi găsită în cele care au avut loc în timpul celui de-al doilea ciclu, care este în care combinația de medicamente a fost primită anterior (în 6 din cele 9 reacții din studiul nostru). Astfel, în utilizarea combinată, ar fi recomandabil să se utilizeze o premedicație completă, să monitorizeze îndeaproape pacienții și să știe cum să diferențieze reacțiile de hipersensibilitate produse de fiecare medicament, pentru a determina agentul cauzal.
referitor la posibilele prejudecăți sau la limitările posibile ale posibilelor Studiul, probabil, incidența reacțiilor ar fi putut fi mai mare, deoarece evaluarea sa constituie o variabilă subiectivă sau moale care depinde de percepția observatorului. Prin urmare, această circumstanță ar fi putut provoca o minoritate de reacții ușoare, deoarece ar fi putut fi neobservate. O altă părtinire care urmează să fie evidențiată, a fost utilizarea a două mărci comerciale diferite ale Docetaxel în diferite faze ale studiului (Taxotere® și Docetaxel Hospira®), precum și o schimbare de formulare în cazul Taxotere®. Același preparat comercial a fost cel care a prezentat toate reacțiile infuresonale (două dintre ele cu formularea antică), deși este adevărat că a fost cea mai folosită (91,5% din perfuzii). Excipienții ambelor mărci comerciale sunt: etanol, polisorbat 80 și acid citric și în cazul Taxotere® în plus Macrogol 300. Compoziția cantitativă a excipienților nu a putut fi obținută din foile tehnice, așa că nu știm dacă marca comercială sau excipienții lui ar putea influența apariția reacțiilor. O limitare importantă a studiului și care trebuie luată în considerare pentru lucrările ulterioare, a fost testele de non-provocare responsabile de serviciul de alergie pentru a putea discerne dacă aparențele au apărut au fost cauzate de principiul activ sau de excipienți.
În cele din urmă, cu rezultatele obținute în acest studiu, măsurile care au fost luate în centrul nostru au fost de a consolida premedicația Docetaxel și fac o administrare lentă de medicament (2-3 ore) în primul și Al doilea ciclu de tratament. Cu paclitaxelul a fost decis să continue cu aceeași metodologie de lucru, așa cum este indicat pe foaia tehnică.
Concluzii
Docetaxel este taxanul care a fost legat de un număr mai mare în mediul nostru de reacții adverse în timpul perfuziei dvs., superior datelor descrise în literatură.
O premedicație adecvată atât în zile, cât și în casa pacientului, este esențială pentru a reduce incidența acestora.
Este esențial să se facă mai multe studii pentru a putea ști exact etiologia acestor reacții și, astfel, să poată aplica măsuri eficiente care să evite apariția lor.
Conflictul de interese
Autorii Declarați să nu aveți niciun conflict de interese.
bibliografie
1. Foi tehnice Docetaxel (Taxotere®) (Access Iunie 2010). Disponibil la: www.agemed.es
2. Fișa tehnică Paclitaxel (Taxol®) (Accesați iunie 2010). Disponibil la: www.agemed.es
3. Bagnall A-M, Forbes C, Lewis R, Golder S, Kleijnen J. O actualizare a unei revizuiri rapide și sistematice a eficacității și a rentabilității taxanelor utilizate în tratamentul cancerului avansat de sân. Institutul Național de Excelență Clinică (Centrul NHS pentru recenzii și diseminare). Universitatea din York, aprilie 2001 (Accesați iunie 2010). Disponibil la: www.nice.org.Regatul Unit / Nicemedia / Live / 11435/32235 / 32235.pdf
4. Gligorov J, Lotz J-P. Farmacologia preclinică a taxanelor: Implicațiile diferențelor. Oncologul. 2004; 9 (supl 2): 3-8.
5. Hennenfent K L, Govindan R. Novel formulări de taxani: o revizuire. Vin vechi într-o sticlă nouă? Analele Oncologiei. 2006; 17: 735-49.
6. TEN TIJE AJ, Verweij J, Loos WJ, Sparreboom A. Efectele farmacologice ale vehiculelor de formulare: Implicații pentru chimioterapia cancerului. Clin Pharmacokinet. 2003; 42 (7): 665-85.
7. Markman M. Gestionarea toxicității Taxane. Suport pentru îngrijirea cancerului. 2003; 11 (3): 144-47.
8. La zi. Baza de Datos. Reacții la perfuzie la chimioterapia sistemică; Ocupubre 2009 (Accesso Marzo 2010). Disponibil EN: http://www.uptodate.com/contents/infusion-reactions-to-systemicchemotherapy
9. Michaud Lb. Metode de prevenire a reacțiilor secundare la cremofor el. Ann Farmacother 1997; 31: 1402-4.
10. Weiss Rb, DoneHower RC, Wiernik Ph și colab. Reacții de hipersensibilitate de la Taxol. J Clin Oncol. 1990; 8: 1263-8.
11. Institutul Național de Cancer Criteriile de toxicitate comună pentru evenimentele adverse (CTCAE) V3.0; Agosto 2006. (Accesso Marzo 2010). Disponibil en: http://ctep.cancer.gov/protocolDevelopment/electronic_applications/docs/ctcaev3.pdf
12. Naranjo ca, Busto U, vânzătorii em, Sandor P, Ruiz I, Roberts Ea și colab. O metodă de estimare a probabilității reacțiilor adverse la medicament. Clin Pharmacol Ther. 1981; 30: 239-45.
13. Seria de îngrijire a sănătății Micromedex. Baza de date de droguri. Seria Thomson (Accesso Marzo 2010). Disponibil EN: www.thomsonhc.com
14. Dizon DS, Schwartz J, Rojan A, Miller J, Pires L, Disilvestro P, și colab. Sensibilitate încrucișată între paclitaxel și docetaxel într-un program de cancer de femei. Ginecol oncol. 2006; 100 (1): 149-51.
15. Markman M, Kennedy A, Webster K, colab. Reacții de hipersensibilitate asociate paclitaxel: Experiența programului de oncologie ginecologică a Centrului Clinic Cleveland Clinic. J Clin Oncol. 2000; 18 (1): 102-5.
16. Castells MC, Tennant Nm, Sloane de, Ida Hsu F, Barrett Na, Hong Di și colab. Reacții de hipersensibilitate la chimioterapie: rezultatele și siguranța desensibilizării rapide în 413 de cazuri. J Alergy Clin Immunol. 2008; 122: 574-80.
17. Feldweg Am, Lee CW, Matulonis UA, Castells M. Desensibilizare rapidă a reacțiilor de hipersensibilitate la paclitaxel și docetaxel: Un nou protocol standard utilizat în 77 de tratamente de succes. Ginecol oncol. 2005; 96: 824-49.
18. Syrigou E, Dannos I, Kotteas E, Makrilia N, Tourkantonis I, Dilana K, colab. Reacții de hipersensibilitate la docetaxel: evaluarea retrospectivă și dezvoltarea unui protocol de desensibilizare. INT Alergii ARCH Immunol. 2011; 156 (3): 320-4.
19. J Lokich J, Anderson N. Paclitaxel Reacții de hipersensibilitate: un rol pentru substituirea docetaxelului. Centrul de Cancer din Boston. Analele Oncologiei. 1998; 9: 573-4.
20. Moon C, Verschraegen CF, Bevers M, Freedman R, Kaudelka AP, Kavanagh JJ. Utilizarea docetaxelului (Taxotere) la pacienții cu hipersensibilitate Paclitaxel (Taxol). Medicamente anticanceroase. 2000; 11 (7): 565-8.
21. Bernstein BJ. Docetaxel ca alternativă la paclitaxel după reacțiile acute de hipersensibilitate. Ann Farmacother. 2000; 34 (11): 1332-25.
22. Baker J, și colab. Efectele secundare legate de docetaxel și managementul acestora. Jurnalul European de Oncologie Nursing. 2009; 13: 49-59.
23. Lee C, Gianos M, Klasterrmeyer WB. Diagnosticarea și gestionarea reacțiilor de hipersensibilitate legate de agenții de chimioterapie cu cancer comună. ANN ALLERGY ASTMMA IMUNOL. 2009; 102 (3): 179-87.
24. Ardavanis a, Tryfonopoulos D, Yiotis I, Gerasimidis G, Baziotis N, Rigatos G. Natura non-alergică a reacțiilor acute de hiper sensibilitate acută indusă de docetaxel. Medicamente anticanceroase. 2004; 15 (6): 581-5.
25. Sánchez-Muñoz A, Mediola Fernández C, Poza Guedes P, Canto Diez G, Bezies Montes S, Cortés Fune H. HiperSensibilidad A Carboplatino Y Paclitaxel: Revissión y Recomendioni Clínicas. Rev oncol. 2002; 4 (2): 68-71.
26. Cortijo-Cascajares S, Jiménez-Cerezo MJ, Herreros de Tejada A. Revissión de Las Reaccions de HiperSnSibilidad A Antineoplásicos. Farm Hosp. 2012; 36: 148-58.
27. Chung ch. Gestionarea premedicațiilor și a riscului de reacție la terapia cu anticorpi monoclonali infuzioni. Oncolog. 2008; 13: 725-32.
28. Markman M, Kennedy A, Webster K, colab. Caracteristicile clinice ale reacțiilor de hipersensibilitate la carboplatină. J Clin Oncol. 1999; 17 (4): 1141-5.