Un gas ideale o gas perfetto è uno in cui la forza di attrazione o respingimento molecolare tra le particelle che lo compongono, pertanto, è considerata insignificante tutto il suo interno L’energia è cinetica, cioè l’energia associata al movimento.
in un gas del genere, le particelle di solito sono abbastanza lontane da alcuni Di altri, anche se di volta in volta colpiscono tra loro e con le pareti del contenitore.
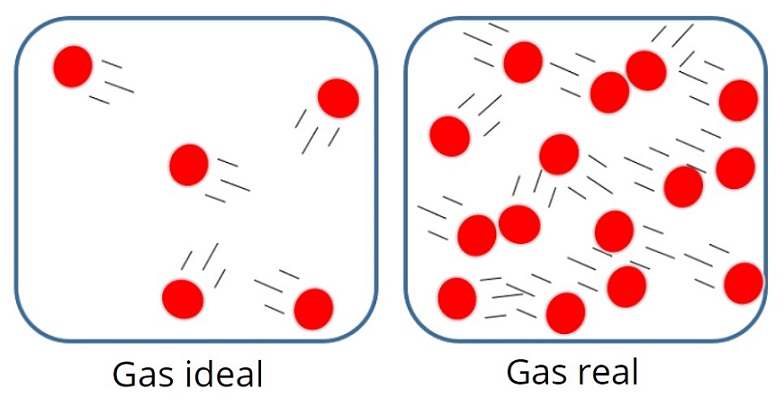
D’altra parte, nel gas ideale non importa la dimensione o la massa delle particelle , poiché si presume che il volume occupato da loro sia molto piccolo rispetto al volume del gas stesso.
è, ovviamente, è solo un’approssimazione, perché in realtà c’è sempre un certo grado di interazione tra gli atomi e Molecole Sappiamo anche che le particelle occupano lo spazio e hanno pasta.
Nonostante queste ipotesi funzionino abbastanza bene in molti casi, come a bassa molecolare gas di peso, in una buona gamma di pressioni e temperature.
Tuttavia, i gas di peso molecolare elevati, soprattutto a pressioni elevate o basse temperature, non si comportano in tutti i gas ideali e altri modelli creati con lo scopo di descrivere loro più accuratamente.
Primi esperimenti
Le leggi che regolano i gas sono empiriche, cioè emerse dalla sperimentazione. Gli esperimenti più notevoli sono stati effettuati nel diciassettesimo secolo, XVIII e all’inizio del diciannovesimo secolo.
Prima di tutto sono quelli di Robert Boyle (1627-1691) e Edme Mariotte (1620-1684), coloro che in modo indipendente Modifica la pressione in un gas e ha registrato il loro cambio di volume, scoprendo che sono stati inversamente proporzionali: a pressione più elevata, volume inferiore.
Da parte sua, Jacques Charles (1746-1823) ha stabilito che il volume e la temperatura assoluta erano direttamente proporzionali , finché la pressione è rimasta costante.
amadeo Avogadro (1776-1856) Scoprì che due volumi identici di diversi gas contenevano il stessa quantità di particelle, purché la pressione e la temperatura erano le stesse. E infine Joseph of Gay Lussac (1778-1850), ha detto che mantenendo il volume fisso, la pressione in un gas è direttamente proporzionale alla temperatura.
Le leggi sui gas ideali
Queste scoperte sono espresse da semplici formule, chiamando pressione, V al volume, n il numero di particelle e la temperatura del gas ideale:
legge di boyle-mariotte
a lungo Poiché la temperatura è fissa, si verifica il seguente:
p⋅v = costante
legge Charles
Quando il gas è sotto pressione costante:
v / t = costante
LUSSSAC legge gay
Mantenere il gas a un volume fisso è vero che:
p / t = costante
Avogadro Law
I volumi di gas identici, sotto le stesse condizioni di pressione e temperatura hanno lo stesso numero di particelle. Pertanto possiamo scrivere:
v α n
dove n è il numero di particelle e α è il simbolo di proporzionalità.
Modello di gas ideale
Il modello di gas ideale descrive un gas tale che:
– Quando le particelle interagiscono fanno per molto tempo, attraverso gli shock elastici, in cui gli impulsi e l’energia sono conservati cinetiche.
-Sus Le particelle costituenti sono puntuali, in altre parole, il suo diametro è molto inferiore alla distanza media che corrono attraverso una e un’altra collisione.
-L’insistenza delle forze intermolecolari sono inesistenti.
-L’energia cinetica è proporzionale alla temperatura.
Gas monatomici -che gli atomi non sono collegati tra peso molecolare sì e basso, in condizioni di pressione e temperatura standard (pressione atmosferica e temperatura 0 º C), Avere un comportamento in modo tale che il modello di gas ideale sia un’ottima descrizione per loro.
Ideal Gas State Equation
Leggi del I gas prima di enunciati sono combinati per formare l’equazione generale che governa il comportamento ideale del gas:
v α n
v α t
Pertanto:
v α n⋅t
in aggiunta, della legge di boyle:
v = costante / p
Possiamo affermare che:
v = (costante xn⋅t) / p
La costante è chiamata costante gase ed è denotato dalla lettera R.Con questa elezione, l’equazione di stato del gas ideale riguarda quattro variabili che descrivono lo stato del gas, vale a dire n, r, p e t, rimanendo:
p⋅v = n⋅r⋅t
Questa equazione relativamente semplice, è coerente con le leggi dei gas ideali. Ad esempio, se la temperatura è costante, l’equazione è ridotta alla legge di Boyle-Mariotte.
la costante del gas
Come abbiamo detto prima, in condizioni standard di temperatura e Pressione, questa è, a 0 ° C (273,15 K) e 1 atmosfera di pressione, il comportamento di molti gas è vicino al gas ideale. In queste condizioni, il volume di 1 molo di gas è 22.414 l.
in tal caso:
r = (p⋅v) / (n⋅t) = (1 ATM x 22.414 L) / (1 MOL x 273.15 K) = 0,0821 ATM ⋅ L / MOL ⋅ K
La costante di gas può anche essere espressa in altre unità, ad esempio nel sistema internazionale se vale la pena :
r = 8,314 j⋅ mol-1⋅ k-1
Quando un problema viene risolto dalla legge dei gas ideali, è conveniente prestare attenzione alle unità in cui La costante è espressa, dal momento che come possiamo vedere, ci sono molte possibilità.
Comportamento di un gas ideale
Come abbiamo detto, qualsiasi gas in condizioni standard di pressione e temperatura e quello È un peso molecolare basso, si comporta molto da vicino il gas ideale. Pertanto, l’equazione p⋅v = n⋅r⋅t è applicabile per trovare la relazione tra le quattro variabili che lo descrivono: n, p, v e t.
In questo modo possiamo immaginare una porzione di gas ideale racchiuso in un contenitore e formato da minuscole particelle, che occasionalmente si scontrano tra loro e con le pareti del contenitore, sempre elastiche.
è ciò che vediamo nella prossima animazione di una porzione di elio, un gas nobile e monoatomico:

Esempi di gas ideali
Un gas ideale è un gas ipotetico, cioè, è un’edilizizzazione , tuttavia, in pratica molti gas si comportano in un modo molto vicino, rendendo possibile per il modello p⋅v = n⋅r⋅t getta risultati molto accurati.
Gas nobili
Esempio di gas che si comportano come ideali in condizioni standard sono gas nobili, oltre a gas leggeri: idrogeno, ossigeno e azoto.
il palloncino aerostatico

Alla mongolfiera della figura 1 La legge Charles può essere applicata: il gas è riscaldato, quindi l’aria che riempie il palloncino Si espande e come conseguenza aumenta.
palloncini di elio
L’elio è, insieme ad idrogeno, l’elemento più comune nell’universo, eppure è scarso sulla terra. Come è un gas nobile è inerte, a differenza dell’idrogeno, ecco perché i palloncini pieni di elio sono molto usati come elementi decorativi.