Intolerancia hereditaria á fructosa (IHF, MIM # 229600) é unha enfermidade recesiva autosómica debido á deficiencia de aldolase B, enzimática a cargo do metabolismo da fructosa, no fígado principalmente .. O consumo de frutosa, sacarosa, sorbitol ou tagatosa1 en pacientes con IHF causa síntomas serios que poden levar a unha hipoglicemia analítica, neurolóxica, hepática, renal, hipoglicemia e mesmo morte2.
presentacións de drogas líquidas orales que se elaborou clásicamente con Sacarosa (xarope simple), pero aumenta o uso doutros edulcorantes, como xaropes hidrogenados (polialcohols) ou, en menor medida, xaropes de glicosa. Os polialcoholes obtéñense pola hidrogenación catalítica de azucres, obtendo produtos con baixa enerxía calórica (maltitol, sorbitol, lactitol, etc.). Pola contra, os xaropes de glucosa son máis calóricos, sendo menores o seu poder de edulcorante, aínda que se pode aumentar ao transformar parte da glucosa de frutosa (isomerización). Na industria alimentaria, se a cantidade de frutosa é superior ao 5%, debe indicarse na definición do ingrediente3. Na industria farmacéutica é obrigatorio dar unha advertencia no prospecto e na folla técnica para pacientes con IHF se a medicación contén fructosa, sacarosa, azucre investido, sorbitol, maltitol, isomaltitol e lactitol, por ser editado contraindicado en IHF4 (Táboa 1 ). Detectáronse erros en follas técnicas na denominación de xaropes de glucosa potencialmente perjudicial para pacientes con IHF.
Características de excipientes / edulcorantes e a súa tolerancia en ihf
| Excipiente | Composición | Sinónimos | obteña | apt on ihf? | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| monosacáridos | ||||||||||
| sorbitol | sorbitol | D-glucitol, d-sorbitol | hidrogenación de glucosa | non | ||||||
| Disacared | ||||||||||
| Sucarosa | glicosa-frutosa | azucre de mesa, azucre común | da azucrecana | non | ||||||
| isomaltitol | mestura de maltitol e glicosa-manitol | isomalta, isomaltol, isomalt, isomaltulosa hidrogenada, palatalinose hidrogenada | Hidrogenación de isomaltura | noa | ||||||
| lactitol | galactosa-sorbitol | lactita, lactositol, lactoblosite | Hidrogenación de lactosa | Noa | Maltitol | Glucose-Sorbitol | Maltosa hidrogenada | Hidrogenación do hidrolizato de amidón | Noa | |
| jarabes | ||||||||||
| azucre invertido | Glucosa e mestura de frutosa | azucre líquido invertido, xarope de azucre invertido | hidrólise de sacarosa | non | ||||||
| Xarope de glicosa | Glucose, Maltosa e Oligosaccharidic Mestura | Xarope de millo | Hidrólise de Starch | Yesb | ||||||
| Maltitol Syrup | Mestura de Sorbitol, Maltitol e polisacáridos hidrogenados | Xarope de glicosa hidrogenada, xarope de glicosa hidrogenada con alto contido en maltosa, hidrolizado hidrogenado (/ td> | Hidrogenación de xarope de glicosa ou hidrolizado de amidón | Noa | ||||||
| Xarope de millo con alto contido en fructosa | Glucosa e frutosa | Isoglucosa, xarope de millo de alta frutosa | hidrólise de amidón de millo e isomerización da glucosa de frutosa (42 -55%) | non | ||||||
A absorción non está completa. Hai controversia na súa tolerancia.
verificar se contén fructosa.
Fonte: Real Farmacoaea español5 e real decreto 299/2009 de marzo de 66.
Para determinar o seu alcance, os chips técnicos de medicamentos que conteñen xarope de glucosa foron revisados entre maio de 2013 e xullo de 2016 coa ferramenta de nomenclator de prescrición da Axencia Española de Medicamentos e Produtos Sanitarios ( www.aemps.gob.es) e a información confirmouse con cada laboratorio fabricante.
Detectouse 42 presentacións comercializadas con xarope de glucosa. 4 presentacións tópicas e 27 foron excluídas que conteñen sacarosa, sorbitol, maltitol, isomaltitol ou xarope de millo con alto contido de fructosa (sen aparecer alerta para IHF en 3 presentacións). Analizamos 11 presentacións: 9 con glucosa líquida e 2 con xarope de glucosa hidrogenada.
Nas 2 presentacións con glucosa líquida e en 2 con xarope de glucosa hidrogenada o laboratorio confirma que conteñen fructosa e maltitol / sorbitol, respectivamente. A formulación destas 4 presentacións está en forma de xarope ou solución oral, o resto son tabletas, cápsulas ou frascos. Nunha presentación indícase que o xarope de glicosa contén 40% de frutosa. En 2 presentacións do mesmo laboratorio, non se obtivo información sobre a composición de glucosa líquida e noutro 3 (27,7%) a primeira resposta obtida foi imprecisa ou contén erros que requirían unha segunda consulta (Figura 1). En calquera caso, o atraso da resposta foi de 4 meses.
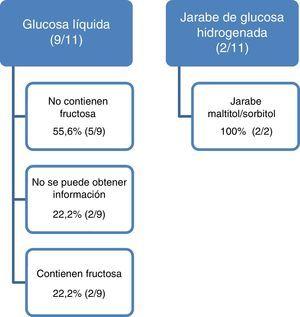
Os resultados obtidos coa información proporcionada polo laboratorio de marcador de medicamentos.
Conclusión, moi grave Detectáronse erros na información sobre excipientes nas follas técnicas implicadas nun grave problema de seguridade para os pacientes con IHF. Os 2 erros máis graves foron:
- –
Indique sobre a folla técnica “xarope de glicosa ou glucosa líquida” cando en realidade é “xarope de glicosa-frutosa”.
Indique sobre a folla técnica “xarope de glucosa hidrogenada” como sinónimo de “xarope de glicosa”, cando en realidade é “xarope de maltitol ou xarope sorbitol”.
Ademais, observouse que non todos os medicamentos que conteñen fructosa, sacarosa, sorbitol, maltitol, isomaltitol ou lactitol conteñen a alerta / contraindicación correspondente a pacientes con IHF no material de acondicionamento O o Cartón, folla técnica e folleto (de acordo coa lexislación sobre etiquetaxe).
A revisión realizouse a través dunha aplicación que filtra os medicamentos segundo excipientes. A pesar diso, non se pode garantir que todos os medicamentos con xarope de glicosa foron revisados. Polo tanto, estes erros foron reportados ao programa de seguridade do paciente e erros de medicación do asesoramento sanitario da comunidade e AEMPS (Errors. [email protected]), para que poida realizar notificacións oportunas para a industria farmacéutica e profesionais da saúde.
A pesar do tamaño da mostra, ambos erros son moi sorprendentes e a dificultade de obter información fiable e precisa do laboratorio do fabricante, sendo necesario, en varios casos, as clarificacións posteriores, que levaron a rectificacións con respecto ao Información emitida anteriormente. Nun dos casos, se a primeira información do fabricante fora considerada correcta, a consecuencia da administración do medicamento en cuestión nun paciente con IHF podería ter consecuencias graves na súa saúde. Necesitamos un proceso de revisión do contido da ficha técnica de forma coordinada entre as axencias reguladoras e as empresas fabricantes e / ou comerciantes destes medicamentos.