Imaxe Radioterapia guiada. Impacto clínico
Impacto clínico da radioterapia guiada por imaxe
p. Romero, E. Villafranca, M. Rico, A. Manrola, M.T. Vila, M. A. Domínguez
Servizo de oncoloxía de radioterapia. Hospital de Navarra. Pamplona.
Dirección de correspondencia
Resumo
A radioterapia guiada por imaxe (RTGI) é un concepto que engloba a forma máis moderna de administrar o tratamento de radioterapia que é o obxectivo Maximizar a dose depositada en volume a ser tratada (obxectivo), minimizando a dose en órganos saudables.
Isto non sería posible sen o desenvolvemento tecnolóxico e software continuo, especialmente nas seguintes áreas: rexistrar imaxes deformábeis, replanar novos tratamentos, imaxe en tempo real e cálculo de dose acumulado.
O impacto clínico é evidente, pero pouco se fala sobre o impacto sobre a reorganización dos servizos de oncoloxía radioterapia. O RTGI supón unha formación de todo o equipo involucrado, cun período de aprendizaxe e posta en marcha. Coa experiencia adquirida, o tempo dedicado a cada paciente (en todas as etapas do seu tratamento: Simulación, planificación, posta en marcha, posicionamento de sistemas de verificación, correccións en liña, fóra de liña, replanning, controis clínicos periódicos), é moito maior que que é necesario na terapia de radiación convencional, que aparecen novas responsabilidades e roles.
Palabras clave: Image Radiación guiada. Radioterapia adaptativa. Cancro de próstata. Cone Beam Ct. Confianza.
Resumo
Imaxe Radioterapia guiada (IGR) é un concepto que engloba a forma máis moderna de administrar o tratamento de radioterapia. O obxectivo é maximizar a dose depositada no volume de destino, minimizando a dose en órganos saudables.
Isto non sería posible sen o desenvolvemento continuo da tecnoloxía e do software, sobre todo nas seguintes áreas: rexistro de imaxe deformable, replanando novos tratamentos, imaxe en tempo real e cálculo de dose acumulada.
Mentres o impacto clínico é evidente, pouco se di sobre o impacto sobre a reorganización dos servizos de oncoloxía da radioterapia. IGr supón a formación de todos os membros do equipo que indican, cun período de adestramento e inicio. Coa experiencia adquirida, o tempo dedicado a cada paciente (en todas as etapas de tratamento: a simulación, a planificación, a partir, os sistemas de verificación de posición, as correccións en liña, fóra de liña, a replanificación, os controis clínicos periódicos) son moito maiores que iso Requerido na radioterapia convencional, que dá lugar a novas responsabilidades e roles.
palabras clave. Imaxe Radioterapia guiada. Radioterapia adaptativa. Cancro de próstata. Cone Beam Ct. Fiduciales.
Introdución
Radioterapia é unha das principais modalidades terapéuticas que existen contra o cancro. De xeito moi sinxelo, o proceso de planificación do tratamento radioterapéutico é delimitar o volume do tumor (obxectivo), chamado GTV (volume de tratamento bruto), CTV (volume de destino clínico) e órganos de risco (ICRU 62).
No proceso de planificación e administración de tratamento radioterapéutico, hai incertezas sistemáticas e aleatorias. Os primeiros débense a erros na planificación e simulación (diferente posicionamento do paciente durante a adquisición de imaxes para planificar o tratamento e durante o posicionamento de tratamento). Estes erros sistemáticos repetiranse ao longo do tratamento. Os erros aleatorios aparecen por desviacións diarias colocando ao paciente, debido a cambios anatómicos na morfoloxía do tumor ou o movemento interno presentado por algúns órganos (por exemplo, o pulmón con movementos respiratorios). Os erros aleatorios prodúcense no momento e durante a administración de tratamento.
Estas incertezas son responsables da existencia de PTV1 (PTV: Planificación Target volume), que é a marxe de seguridade adecuada que ten que proporcionar o obxectivo Para garantir que reciba a dose prescrita.
En radioterapia convencional, a verificación de posicionamento está feita con imaxes planas de MegaVoltage baseadas en referencias óseas, sen visualizar os tecidos brandos (obxectivo e / ou remo), aumentando así as incertezas .. É por iso que os PTV entran en conflito co remio, limitando así a escalada de dose.
O RTGI supón un avance en precisión e mellora da capacidade de oncólogo radiótica para aumentar a dose de forma segura e efectiva. Axuda a localizar e concentrar o obxectivo cunha velocidade e precisión adecuada, o que permite modificar con precisión e adaptar o tratamento de Daily2.3.
Sistemas de imaxe guiados
Debido a cambios anatómicos que experimentan o Obxectivo, é necesario obter imaxes que garantan a precisión do tratamento.Estas imaxes poden ser:
– Imaxes 3D planas: Imaging de portal electrónico Megavoltage ou dispositivos Kilovoltage (KV) para mostrar marcadores de radiopaco.
– Imaxes volumétricas: ultrasóns, tomografía computada.
– 4D imaxes (obter información anatómica en referencia aos cambios producidos pola respiración) En tempo real, na sala de tratamento, é a base do RTGI.
Cando recibe unha imaxe ten que comparalo coa referencia (normalmente é unha imaxe plana radiográfica KV, que equivale á reconstrución dixital radiográfica (RDR ), xerado no planificador da Simulación TC. Esta imaxe de referencia ou as imaxes da simulación TC son aquelas que se usan para comparar e verificar o posicionamento do paciente ou o obxectivo no momento da administración do tratamento radioterapéutico. Se se compara só no tempo que o fas e anteriormente Para iniciar o tratamento, chámase verificación en liña. As modificacións realizadas neste momento, corrixir erros sistemáticos e aleatorios, polo tanto, o día do inicio e os cambios en fase, a verificación en liña sempre se realiza. Os protocolos de corrección en liña requiren a presenza do oncólogo de radioterapia, que decide a modificación e determina o momento e o número de controis en liña. Se a verificación de imaxe realízase unha vez que se administra o tratamento, denomínase verificación fóra de liña. Este tipo de verificación corrixe os erros sistemáticos estimados durante a fase inicial do tratamento nas fases posteriores. Os protocolos sen conexión son os máis utilizados, o chamado nivel de acción shinrinking (SAL) e sen nivel de acción (NAL).
A comparación destas imaxes é fundamental e pode levar a non ter que realizar calquera desprazamento ; O outro extremo é ter que replanar o tratamento por cambios importantes na xeometría do obxectivo5 ou o movemento diario. A posibilidade de medir e xestionar estes erros dependerá do sistema RTGI usado. A continuación descríbese os principais sistemas de imaxe guiados:
1. Marcadores RIOPHAC (fiduciales) de diferentes materiais (ouro, prata), dimensións (2 mm-10 mm) e formas (esferas, sementes cilíndricas) (Fig. 1), implantados no tecido brando permiten ao obxectivo directamente. A principal aplicación clínica é o tratamento da próstata Tumor4, tamén en páncreas e pulmón. Son facilmente identificados nunha imaxe radiográfica plana, facilitando a decisión de corrixir o posicionamento e a rapidez da liña na obtención da imaxe. O principal problema é que poden migrar e a ausencia de información sobre as posibles deformacións dos tecidos que manteñen o tumor ou a barra preto.

2. Ultrasound. Obtén imaxes volumétricas. A súa principal aplicación clínica está no tumor da próstata. Presenta a súa innovación como unha seguridade e unha fácil visualización da próstata. Os inconvenientes son: proporciona imaxes diferentes ás do TC do simulador, unha importante variabilidade de interobreserver ea posible modificación da morfoloxía da próstata coa presión da próstata.
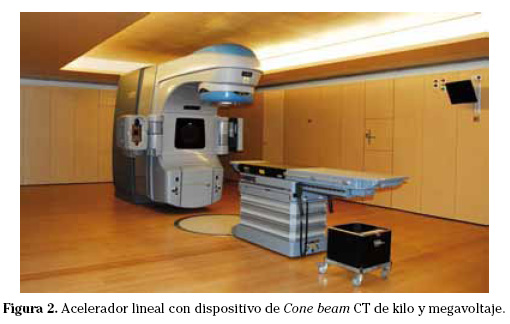
3. Tomografía calculada polo feixe de cono (CBCT) (Fig. 2). Permite obter imaxes de tomografía axial na sala de tratamento, facilitando a comparación coas imaxes da simulación TC. Consiste nun feixe cónico (cono beat) equipo montado na liña do acelerador lineal, que obtén imaxes volumétricas nunha única rotación do tubo de raios X e Detector. O seu principal problema é o longo tempo de adquisición das imaxes (aproximadamente un minuto) e que a respiración pulmonar artesanía unha morea de imaxes especialmente as do tórax e do abdome.
4. En estudo: Sistemas guiados por fluoroscopia, tomosíntese e sistemas electromagnéticos. Moi interesante o futuro da integración da imaxe magnética de resonancia en tratamento radioterapico5.
Aplicacións clínicas
Comparando o erro residual (a desviación que permanece despois de corrixir o posicionamento da posición planificada) con cada un Sistema de imaxe guiada en tumores de próstata6, o menor erro residual xera (uns 2 mm) é a imaxe diaria con CBCT con referencia de tecido brando e CBCT con fiducial. No caso do tumor de pulmón7, os movementos respiratorios complican as imaxes. O erro residual, cun esquema hipofraccionista e marco do corpo de inmobilización, é un inmovilizador que proporciona un sistema de presión abdominal para diminuír o desprazamento debido ao movemento respiratorio (Fig. 3) e imaxes diarias de CBCT con referencia do tumor. Obtense erros de 3 mm (media da posición do tumor respecto da respiración).Na cabeza e os tumores de pescozo, o erro residual, utilizando imaxes radiográficas, é de > 5 mm en 10% dos pacientes se se realiza diariamente, por outra banda, se se realiza semanalmente, Este erro é obxectivo no 33% dos pacientes. Neste tipo de tumores, a replanificación9 é importante, porque hai unha diminución do tamaño do tumor (media do 69%), o tamaño das glándulas parótidas (28%) e os ganglios linfáticos, desprazando o posicionamento de órganos saudables a Áreas de dose alta. Isto adquire máis importancia, se é posible, cando se usa a técnica de radioterapia de intensidade modulada.

Ao combinar a intensidade modulada RTGI e Radioterapia, o As ferramentas son necesarias para administrar altas doses / fracción, a chamada hipofracción, acurtando así o tempo de tratamento e garantindo un tratamento eficaz e seguro. Os protocolos de verificación en liña son clave neste tipo de tratamentos. Existen estudos clínicos10 en curso pendentes de resultados definitivos. As aplicacións clínicas máis estudadas están en lesións parasas11, pulmón tumor12 e tumor intrahepático13. En lesións parasinales, o erro residual entre as imaxes de KV planas compárase cos do CBCT, sendo 2,3 mm e 1,5 mm respectivamente. Co CBCT, as rotacións son mellor detectadas, mesmo con inmobilizadores en “berce” de pacientes. No caso das lesións intrahepáticas, tamén se observa unha vantaxe no erro residual da imaxe volumétrica co CBCT con respecto á imaxe plana, mellorando a dose nas estruturas vasculares e dutos intrahepáticos saudables. O control de calidade destes equipos debe ser exhaustivo, incluíndo tolerancias e periodicidade14.
Consideracións xerais
A precisión do posicionamento do obxectivo está influenciado polo sistema de imaxe guiado e do protocolo de Corrección. Co RTGI, débense as condicións para planificar os tratamentos cun índice de alta conformación e conseguir con gran precisión a localización do obxectivo e delimitación dos volumes de interese.
Para facer cambios na práctica clínica, como reducir O tamaño do PTV, aumenta a dose total ou a establecer tratamentos hipofractionais, debemos identificar e controlar as incertezas e garantir a súa reproducibilidade durante o tratamento. A calidade das imaxes obtidas cos diferentes sistemas IGRT son clave para facer correccións de posicionamento e adaptar o tratamento inicialmente planificado ás modificacións diarias.
Todo o que comentou non sería posible sen o equipo formado por: Radioterapia , radiofísico, dosimetristas oncólogos, radioterapia e técnicos de enfermaría.
A reorganización do servizo de oncoloxía radioterapia é estrictamente necesario coa posta en marcha de RTGI. Os tempos necesarios para todo o proceso de tratamento de radioterapia (simulación, planificación, protocolos de corrección en liña e fóra de liña, replanning, control periódico dos pacientes) son superiores ás da radioterapia convencional. Novos roles e novas responsabilidades que afectan a todos os empregados implicados no proceso de tratamento radioterapéutico, na súa planificación, posta en marcha e seguimento de pacientes.
Debido ao importante impacto clínico do RTGI, en conxunto co Técnica de modulación de dose, o beneficio clínico debe ser confirmado, que debe ser demostrado nos distintos estudos aleatorios que están en proceso de presentación de resultados.
Bibliografía
1. Bortfeld T, Jiang SB, Rietzel E. Efectos do movemento da distribución total da dose. Semin Radiat Oncol 2004; 14: 41-51.
2. Jaffray Da. Terapia de radiación guiada por imaxe: desde o concepto á práctica. Radia semin Oncol 2007; 17: 243-244.
3. Shirato H, Shimuzu S, KunieDa T, Kitamura K, Van Herk M, Kagei K et al. Aspectos físicos do sistema de seguimento do tumor en tempo real para a radioterapia gated. Int J Radiat Oncol Biol Phys 2000; 48: 1187-1195.
4. Van der Heide A, Kotte An, Denhad H, Hofman P, Lagenijk JJ, Van Vulnn M. Análise da posición baseada no marcador fiducial con verificación de próstata na radioterapia externa do cancro de próstata. Radiother oncol 2007; 82: 38-45.
5. Raymakers BW, Raijmakers AJ, Kotte An, Lagendijk JJ. Integración ao escáner MRI con acelerador de radioterapia de 6 mv. Deposición de dose en campo transversal. Phys Med Biol 2004; 49: 4109-4118.
6. Serago CF, Buskirk SJ, Igel TC, GALE AA, SERAGO NE, EARLE JD. Comparación da imaxe diaria de MegaVoltaje Electronic Portal ou Kilovoltage Imaging con sementes de marcador a imaxes de ultrasóns ou marcas de pel para a localización de próstata e posicionamento de tratamento en patantes con cancro de próstata. Int J Radiat Oncol Biol Phys 2006; 65: 1585-1592.
7.Chang J, Mageras G, Yorke E, De Arruda F, Sillanpaa J, Rosenzweig Ke et al. Observación das variacións interfraccionais na posición do tumor pulmonar usando a tomografía computable de Tomografía Computada de Tomografía COMPUCUACIÓN RESPIRATORIA E MAGAVOLTAJE. Int J Radiat Oncol Biol Phys 2007; 67: 1548-1558.
8. ZEIDAN OA, LANGEN KM, Meeks SL, Manon RR, Wagner Th, Willoughby Tr et al. Avaliación de protocolos de Image-Guiadance no tratamento de cancros de cabeza e pescozo. Int J Radiat Oncol Biol Phys 2007; 67: 670-677.
9. Kuo C, Wu Th, Chung Ts, Huang KW, Chao KS, Su WC et al. Efecto da regresión de ganglios linfáticos agrícolas sobre as doses de radiación recibidas por glándulas parótidas durante a radioterapia modulada pola intensidade para o cancro de cabeza e do pescozo. AM J Clin Oncol 2006; 29: 600-605.
10. Carey Sampson M, Katz A, Constine LS. Terapia de radiación corporal estereotáctica para oligometastasas extracraneas: a espada ten bordo dobre? Semin Radiat Oncol 2006; 16: 67-76.
11. Yamada y, Lovelock M, Bilsky MH. Terapia de radiación modulada pola intensidade por imaxe de tumores de espiña. Curr neurol neurosci Rep 2006; 6: 207-211.
12. Timmerman Rd, Forster Km, Chinsoo Cho L. Entrega de radiación esteretáctica extracraniana. Radia de semin Oncol 2005; 15: 202-207.
13. Balter M, Brock KK, Litzenberg DW, Mc Shan DL, Lawrence Ts, Ten Haken R et al. Orientación diaria de tumores intrahepáticos de radioterapia. Int J Radiat Oncol Biol Phys 2002; 52: 266-271.
14. Bissonnenette JP. Garantía de calidade das tecnoloxías de orientación de imaxes. SonMon Radiat Oncol 2007; 17; 278-286.