ORIGINALS
Estudi de les reaccions adverses relacionades amb la infusió de paclitaxel i docetaxel
Study on the adverse reactions related to paclitaxel and docetaxel infusion
I. J. Castro1, M. Pons Busom1, GI Ballesteros Cabañas1, I. Ramió Montero1, A. Álvarez Méndez2, R. De Castro Chivato3, M. Centelles Ruiz4
1Servei de Farmàcia, Capio Hospital Universitari Sagrat Cor, Barcelona, Espanya.
2Enfermera Servei de Farmàcia, Capio Hospital Universitari Sagrat Cor, Barcelona, Espanya.
3Enfermera Hospital de Dia, Capio Hospital Universitari Sagrat Cor, Barcelona, Espanya.
4Servicio d’Oncologia, Capio Hospital Universitari Sagrat Cor, Barcelona, Espanya.
Aquest treball va ser presentat parcialment com a comunicació tipus pòster en el 56 Congrés Nacional de la Societat Espanyola de Farmàcia Hospitalària que es va celebrar a Santiago de Compostel·la de l’18 a el 21 d’octubre del 2011.
Direcció per a correspondència
RESUM
Objectiu: Determinar la incidència de reaccions a la infusió de paclitaxel i docetaxel , i les possibles causes que poden desencadenar-les.
Mètode: Estudi de cohorts de les infusions de paclitaxel i docetaxel realitzades en un hospital de tercer nivell, des de juliol de 2010 fins a desembre de 2011 (18 mesos). Per a cada infusió es van registrar les dades clíniques de l’pacient i els referents a l’taxano administrat. Davant l’aparició d’una reacció durant la infusió es va especificar: tipus, gravetat i si aquesta va obligar a la suspensió de l’tractament. Es van consultar les històries clíniques i les ordres mèdiques. El seguiment de les infusions es va realitzar contactant amb les infermeres d’hospital de dia. Es va efectuar un estudi descriptiu de les variables més rellevants incloses en el seguiment i es va analitzar si alguna d’elles podia influir en l’aparició de reaccions.
Resultats: Durant el període d’estudi, es van administrar 357 infusions de paclitaxel i docetaxel a 92 pacients: mitjana d’edat 61,4 anys (DE 11,1), 50,0% dones. Es van detectar 9 reaccions infusionals que van afectar a 8 pacients, totes elles causades per docetaxel (χ2 = 8,3, p = 0,004); el 14,5% dels pacients que el van portar, i sempre durant el primer o segon cicle de tractament. Les variables associades significativament a l’aparició de reaccions van ser: neoplàsia de pulmó (p < 0,005), esquema docetaxel-cisplatí (p < 0,005 ), rebre el fàrmac en primera línia (p = 0,021) i malaltia no avançada (p = 0,014). Conclusions: En el nostre centre hospitalari, docetaxel és el taxano que ha provocat més problemes de seguretat durant la seva infusió.
Paraules clau: Paclitaxel; docetaxel; Reacció d’hipersensibilitat.
ABSTRACT
Objectiu: To determini the incidence of paclitaxel and docetaxel infusion-associated reactions, and the likely causes that may trigger them.
Method: Cohort study of the paclitaxel and docetaxel infusions Carried out at a Tertiary hospital from July of 2010 to December of 2011 (18 months). For each infusion, the clinical data and the drug-related data were recorded. When a reaction occurred during the infusion the following data were specified: type, severity, if treatment withdrawal was needed. The clinical charts and treatment orders were reviewed. The follow-up of the infusions were done by Contacting the day-care hospital nurses. A descriptive study was done for the most relevant variables inclòs in the follow-up and we analyzed if any of them could have had an influence on the occurrence of the reactions.
Results: During the study period, 357 paclitaxel and docetaxel Infusions were administered to 92 patients: pixen age 61.4 years (SD 11.1), 50.0% were female. 9 infusion reactions affecting 8 patients occurred, all of them caused by docetaxel (χ2 = 8.3, p = 0.004); 14.5% of the patients receiving it, and always during the first or second treatment cycle. The variables significantly associated to the occurrence of the reaction were: lung cancer (p < 0.005), docetaxel-cisplatin regime (p < 0.005 ), receiving the drug es first line (p = 0.021), and non-advanced disease (p = 0.014).
Conclusions: At our hospital, docetaxel is the taxane that has Provoked the most freqüent safety problems during the infusion.
Key words: Paclitaxel; docetaxel; Hypersensitivity reaction.
Introducció
Des de ja fa algunes dècades, els taxans paclitaxel i docetaxel han demostrat ser efectius en una gran varietat de tumors. Paclitaxel està aprovat per al tractament de les neoplàsies de mama, pulmó (cèl·lules no petites) i ovari; i docetaxel per a les de mama, pulmó (cèl·lules no petites), cap i coll, adenocarcinoma gàstric i próstata1,2.L’acció citotòxica dels taxans se sustenta en l’estabilització de la tubulina i la posterior formació de microtúbuls no funcionals que desencadenen una mitosi errònia, de manera que les cèl·lules canceroses deixen de dividir-se i acaben per morir1-3. En estudis preclínics, docetaxel ha demostrat ser més eficaç que paclitaxel ja que s’uneix a la tubulina amb major afinitat, presenta una acció directa antitumoral per activació de vies apoptòtiques i una major retenció en les cèl·lules tumorales4.
Un dels inconvenients que presenten aquestes substàncies és la seva pobra solubilització, per això requereixen l’ús de vehicles surfactants no iònics per a la seva formulació. El Cremophor EL, derivat polioxietilado de l’oli de ricí, és el solubilitzant usat per paclitaxel i el polisorbat 80 (Tween 80), un altre derivat polioxietilado, ho és per a docetaxel. Aquests dos vehicles incrementen les interaccions farmacològiques amb altres antineoplàstics (p. Ex. Antraciclines) i poden alterar la farmacocinètica dels fàrmacs amb els quals es formulen, predisposant a una major toxicitat, especialment en el cas de paclitaxel per la seva farmacocinètica no lineal4-6 . Per minimitzar les reaccions adverses, evitar la premedicació i disminuir els temps d’administració de paclitaxel i docetaxel, s’han desenvolupat noves estratègies de formulació com ara nanopartícules d’albúmina, poliglutamatos, profàrmacs, emulsions o liposomas5. Fins ara, només la nova formulació de paclitaxel a força de nanopartícules d’albúmina (Abraxane®) s’ha comercialitzat a Espanya.
El perfil de seguretat d’aquests agents antitumorals és divergent; mentre paclitaxel està més associat a neuropaties perifèriques, miàlgies i artràlgies, docetaxel ho està a la retenció de líquids (augment de pes, inflamació dels turmells o de la zona abdominal) 5,7. Aproximadament amb la mateixa freqüència, els dos fàrmacs poden provocar reaccions a la infusió (dispnea, dolor toràcic, angioedema, hipotensió, urticària i rash cutani) que depenen de les pròpies característiques de l’taxano, de l’solvent o de tots dos, i l’aparició és possible que s’hagi de, entre altres causes, a la infusió ràpida d’aquests preparados8,9. Aquestes reaccions, moltes vegades també anomenades reaccions d’hipersensibilitat, solen ocórrer durant els primers minuts d’infusió i generalment en la primera o segona dosi, podent aparèixer fins i tot amb una adequada premedicació basada en corticoides i antihistamínicos8,10.
tot això ha motivat el nostre interès per determinar la incidència de reaccions adverses relacionades amb la infusió dels taxans paclitaxel i docetaxel en el nostre centre, i les possibles causes que poden desencadenar-les.
Mètode
estudi observacional, longitudinal i prospectiu de totes les infusions de paclitaxel o docetaxel des de juliol de 2010 fins a desembre de 2011, en un hospital universitari de nivell 3 sense trasplantaments.
Els pacients tractats amb paclitaxel van rebre premedicació oral amb dexametasona 8 mg el dia previ a la quimioteràpia, i el mateix dia per via intravenosa: ondansetron 8 mg, dexametasona 8-12 mg, dexclorfeniramina 5 mg i ranitidina 50 mg, 30 minut us abans de la seva administració. La premedicació usada per docetaxel va consistir en dexametasona oral 8mg dues vegades a el dia durant tres dies, iniciant un dia abans de la quimioteràpia, ia més, el mateix dia per via intravenosa: ondansetron 8 mg i dexametasona 8-12 mg, 30 minuts abans de la seva administració.
Les marques comercials utilitzades van ser paclitaxel Hospira® en el cas de paclitaxel i Taxotere® i docetaxel Hospira® per docetaxel. Docetaxel es va administrar en sèrum fisiològic de 250 ml durant 60 minuts, i paclitaxel en sèrum fisiològic de 500 ml en 180 minuts d’infusió. A la poliquimioteràpia, els taxans van ser administrats sempre en primer lloc, de manera que les reaccions que poguessin aparèixer durant els primers minuts d’infusió només podien ser atribuïdes a aquests.
Es va realitzar un seguiment diari de totes les administracions de taxans i es van registrar els següents variables:
• Dades de l’pacient: edat, sexe, número d’història clínica i oncòleg responsable.
• Dades clíniques: neoplàsia, estadi, antecedents patològics, al·lèrgies, medicació habitual i tractaments quimioteràpics previs en el cas que n’hi hagués.
• Dades referents a l’tractament oncològic: tipus de taxano (incloent nom comercial) , dosi, freqüència, cicle, quimioteràpia concomitant i premedicació.
• Aparició d’alguna reacció adversa medicamentosa (RAM) durant la infusió de l’taxano, especificant tipus i gravetat d’acord amb la classificació NCI-CTCAE v.3.0 2006 de National Cancer Insitute11 .
Per registrar les dades relacionades amb el pacient es van consultar les històries clíniques.Les dades referents a l’tractament oncològic es van obtenir de la recepta mèdica per pacient i cicle de tractament. El seguiment de cada infusió va ser realitzat pel farmacèutic responsable de l’àrea de citostàtics i el farmacèutic resident contactant amb la infermera d’hospital de dia encarregada d’administrar el taxano. La relació de causalitat de les reaccions va ser determinada mitjançant l’algoritme de Karch-Lasagna modificado12.
L’anàlisi estadística de les variables qualitatives i quantitatives es va realitzar amb el programa SPSS v.15.0. Es va avaluar si la variable dicotòmica principal RAM si -RAM no, s’associava o no de manera significativa amb cadascuna de les variables independents. La prova de chi-quadrat es va emprar per a les variables categòriques i la t d’Student per a la comparació de mitjanes en mostres independents, prenent p < 0,05 com a relació estadísticament significativa.
l’estudi va ser aprovat pel Comitè Ètic d’Investigació Clínica de l’hospital i va requerir per a la seva realització la signatura de consentiment informat per part dels pacients que complien els criteris d’inclusió.
Resultats
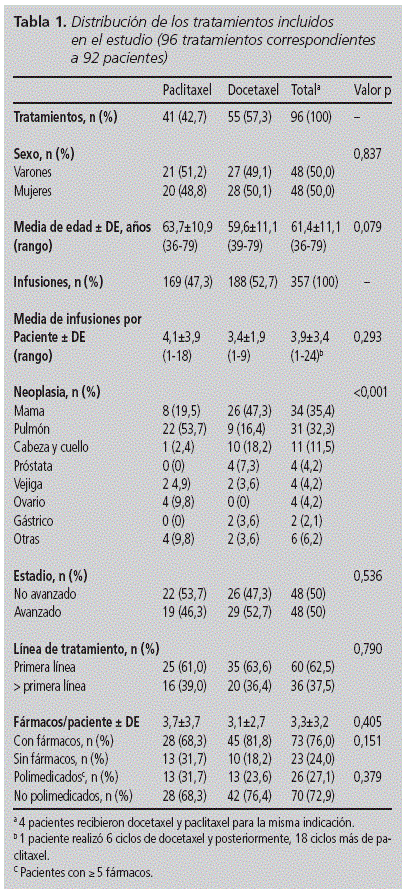
Durant els 18 mesos d’estudi es van infondre 4.689 fàrmacs oncològics, dels quals el 7,6% van correspondre als taxans inclosos en el seguiment. En total 357 infusions de paclitaxel i docetaxel administrades a 92 pacients (50,0% dones), amb edats compreses entre 36 i 79 anys, i una mitjana d’edat de 61,4 anys (DE 11,1). Docetaxel va ser el taxano més utilitzat tant en nombre de pacients (n = 55, 57,3%) com de infusions (n = 188, 52,7%). No es van trobar diferències significatives en les variables basals de les dues cohorts, a excepció de la distribució de les neoplàsies (taula 1): la indicació més habitual per docetaxel va ser el càncer de mama (47,3%), mentre que per paclitaxel va ser el de pulmó (53,7%). Més de la meitat dels pacients van rebre el tractament en primera línia (62,5%).
Es van utilitzar un total de 36 protocols quimioteràpics, sent l’esquema més emprat tant per docetaxel com per paclitaxel la combinació amb carboplatí (càncer de cap i coll, i pulmó respectivament) (taula 2).
Es van detectar 9 reaccions infusionals corresponents a 8 pacients (8,7% de l’total), totes elles causades per docetaxel (χ2 = 8,3, p = 0,004) i sempre durant el primer o segon cicle de tractament. Així doncs, el 4,8% de les infusions de docetaxel van ocasionar una reacció, el 66,7% (n = 6) de les quals van aparèixer en el segon cicle de tractament i van acabar afectant el 14,5% dels pacients que havien rebut aquest quimioteràpic. Si se seleccionen només les infusions de docetaxel administrades durant el primer o segon cicle, la incidència de reaccions s’incrementa fins al 10,5% de les administracions. En tots els casos, les reaccions van aparèixer en pacients amb una edat inferior a 65 anys (56,3 anys D’4,1), no polimedicats, sense al·lèrgies prèvies conegudes i en primera línia de tractament.
El 66,7% (n = 6) de les reaccions van ser considerades com moderades segons el NCI-CTCAE v.3.011. En un dels casos la reacció va ser considerada com a molt greu ja que es van requerir mesures de suport vital. Aquest va ser l’únic cas en què la reacció va motivar la suspensió de l’tractament. En 6 pacients el retractament amb docetaxel va ser tolerat sense problemes i en dos pacients es va administrar paclitaxel posteriorment sense incidències (taula 3). Segons l’algoritme de Karl-Lasagna modificado12 totes les reaccions van ser classificades com a probables.
En el grup dels homes van aparèixer 5 reaccions que van tenir com a denominador comú el càncer de pulmó i l’esquema docetaxel 75 mg / m2 + cisplatí 75mg / m2 c / 21 dies. Aquest esquema va ser administrat a un total de 6 pacients, de manera que el 83,3% dels que van rebre aquest protocol van presentar una reacció a la infusió. En les 3 reaccions que van aparèixer en dones, l’única neoplàsia implicada va ser la de mama, i els protocols quimioteràpics van ser en 2 ocasions la combinació amb trastuzumab i en una amb carboplatí.
En aquest estudi les variables que es correlacionar estadísticament amb l’aparició de reaccions a la infusió de docetaxel van ser: neoplàsia de pulmó (p < 0,005), esquema docetaxel-cisplatí (p < 0,005), rebre el fàrmac en primera línia (p = 0,021) i en malaltia no avançada (p = 0,014). No obstant això no es va observar tal correlació amb les variables sexe, edat i medicació habitual.
Discussió
L’efectivitat dels taxans es pot veure compromesa per l’aparició de reaccions d’hipersensibilitat durant la seva infusió. De vegades aquestes poden obligar a suspendre el tractament havent de recórrer a altres esquemes que podrien ser menys efectius.
A la literatura científica es descriu que docetaxel i paclitaxel provoquen reaccions d’hipersensibilitat amb una freqüència propera a l’30%, però disminueix fins al 2-5% si es realitza pretractament amb corticoides i antihistamínics, i si es redueix la velocitat de perfusión1,2,8,13,14. En el nostre estudi, paclitaxel no va provocar cap reacció amb la premedicació utilitzada i infundiéndolo durant 3 horas2. No obstant això, amb docetaxel van aparèixer 9 episodis (14,5% dels pacients) administrant durant una hora i malgrat administrar a Hospital de Dia la premedicació recomanada en fitxa técnica1. La majoria de les reaccions (6) van ser solucionades reforçant la premedicació, i reduint la velocitat d’administració de 250 ml / h a 125 ml / h i incrementant posteriorment la velocitat de forma progressiva. Alguns autors, a part de reduir la velocitat d’administració també recomanen altres opcions com disminuir la concentració de fàrmac a administrar o bé considerar l’aplicació de protocols de desensibilització mitjançant perfusions amb dosis crecientes15-18. Hi ha estudis que advoquen també per canviar un taxano per un altre quan apareix una reacció d’hipersensibilitat a un ellos19-21. Certament, el canvi d’un per un altre pot afavorir la continuació de l’tractament, però existeix controvèrsia a l’respecte ja que altres autors com Dizon et al.14 opinen que això no és possible per l’existència d’una reactivitat creuada entre els taxans. En el nostre seguiment no va haver tal reactivitat creuada, ja que dos pacients que van presentar una reacció infusional a docetaxel van rebre posteriorment paclitaxel sense incidències. En 6 pacients el retractament amb docetaxel va ser ben tolerat, però, hi va haver un pacient que després de presentar una reacció moderada a docetaxel, va tornar a rebre aquest taxano i novament va presentar una reacció, aquesta vegada considerada com a greu i que va ocasionar la suspensió definitiva de l’tractament . En qualsevol cas, el que sí està clar és que l’administració de qualsevol taxano queda contraindicada si la reacció d’hipersensibilitat ocasionada per algun d’ells és severa (grau 3-4) 1,2.
Els símptomes relacionats amb aquestes reaccions solen aparèixer a la primera o segona infusió de la quimioteràpia i, generalment, als pocs minuts d’iniciar-la, tal com va succeir en els 9 pacients afectats en el nostre seguiment. Per tant, s’ha de prestar especial atenció en les primeres administracions de l’taxano, disposant en tot moment de personal experimentat i el suport d’un equip de reanimació en el cas que hi hagués una reacció que amenaci la vida de l’paciente22. Altres cures que es podrien realitzar són el monitoratge de la pressió arterial i l’observació de l’pacient fins a 2 hores després de l’administració de l’taxano.
En el nostre estudi, la simptomatologia de l’pacient que va tenir una reacció infusional a docetaxel molt greu es va caracteritzar per cianosi, pèrdua de consciència, crisi comicial, insuficiència respiratòria i hipotensió. El quadre es va revertir ràpidament després de parar la infusió i amb l’ajuda de corticoides, oxigenoteràpia i fluidoteràpia; aquesta reacció va ser notificada a centre de farmacovigilància regional. En els altres casos més lleus les reaccions van consistir en eritema cutani, rubor facial, dolor lumbar, taquicàrdia i en alguns casos calfreds, hipotensió i mareig. En cap d’ells va haver-hi dispnea o broncoespasme.
Dos dels pacients que van presentar una reacció d’hipersensibilitat a docetaxel van reconèixer no haver pres correctament la dexametasona pautada el dia previ a la quimioteràpia (pacients 1 i 2, taula 3 ). No hi ha cap dubte, que per reduir el risc d’aparició d’aquests esdeveniments és clau conscienciar els pacients de la presa adequada de la premedicació que se’ls pauta. Administrar una premedicació basada en antihistamínics i corticosteroides prèvia a l’taxano és d’elecció ja que ha demostrat reduir la incidència i severitat de la retenció de líquids, així com la gravetat de les reaccions de hipersensibilidad1,2,7. A més, evita interrupcions en el tractament i permet incrementar les dosis acumulatives mitjanes dels taxanos8.
Es desconeix si aquestes reaccions depenen de l’solvent, o de l’taxano, o de tots dos components. Tampoc se sap amb certesa el mecanisme pel qual apareixen. Es pensa que poden estar intervingudes per l’activació de l’complement, alliberament inespecífica d’histamina, producció d’òxid nítric o bé per l’alliberament de citocines. Contràriament al que succeeix amb els derivats de l’platí, en principi no es relaciona la seva aparició amb un mecanisme mediat per les IgE, ja que les reaccions solen aparèixer als pocs minuts d’iniciar la infusió durant el primer o segon cicle de tractament, el que suggereix que no hi ha necessitat d’una sensibilització previa23-25.Un altre aspecte a tenir en compte, i que amb la bibliografia consultada no s’ha pogut dilucidar amb exactitud8,26, és determinar si hi ha aspectes clínics o subjectius que puguin predisposar a l’pacient a una reacció d’hipersensibilitat aguda oa qualsevol altra RAM.
en el nostre estudi els factors que es van relacionar estretament amb l’aparició de reaccions infusionals van ser: neoplàsia de pulmó, esquema docetaxelcisplatino, rebre el fàrmac en primera línia i malaltia no avançada. D’aquests factors, en la bibliografia consultada únicament rebre docetaxel en primera o segona línia ha estat considerat com a variable decisiva en l’aparició d’aquestes reaccions.
D’altra banda, hi ha la possibilitat que l’ús concomitant de paclitaxel o docetaxel amb altres antineoplàstics com trastuzumab, carboplatí o cisplatí, pugui potenciar l’aparició de reaccions d’hipersensibilitat, ja que aquests per si mateixos també poden originarlas. Trastuzumab, com els taxans, sol provocar aquestes reaccions en el primer o segon cicle, però aquestes no es presenten als pocs segons d’iniciar la infusión27. En canvi, les reaccions dels derivats de l’platí ocorren majoritàriament a partir de l’sisè cicle, durant o posteriorment a la seva infusión25,28. En el nostre estudi, totes les reaccions van aparèixer en pacients en tractament poliquimioterápico amb aquests fàrmacs: 6 a combinació amb cisplatí, 2 amb carboplatí i 1 amb trastuzumab. No obstant això, només es pot trobar relació a aquelles esdevingudes durant el segon cicle, que és en el que s’ha rebut amb anterioritat la combinació de fàrmacs (en 6 de les 9 reaccions en el nostre estudi). Així doncs, en l’ús combinat seria recomanable fer servir una premedicació completa, monitoritzar estretament els pacients i saber diferenciar les reaccions d’hipersensibilitat produïdes per cada fàrmac, per determinar l’agent causal.
En referència als possibles biaixos o limitacions de l’estudi, probablement la incidència de reaccions va poder haver estat més gran a causa de que la seva avaluació constitueix una variable subjectiva o tova que depèn de la percepció de l’observador. Per tant, aquesta circumstància va poder haver provocat una infranotificació de reaccions lleus perquè van poder haver passat desapercebudes. Un altre biaix a destacar, va ser la utilització de dues marques comercials diferents de docetaxel en diferents fases de l’estudi (Taxotere® i Docetaxel Hospira®), a més d’un canvi de formulació en el cas de Taxotere®. Aquest mateix preparat comercial va ser el que va presentar totes les reaccions infusionals (dues d’elles amb la formulació antiga), si bé és cert que va ser amb diferència el més utilitzat (91,5% de les infusions). Els excipients de les dues marques comercials són: etanol, polisorbat 80 i àcid cítric, i en el cas de Taxotere® a més Macrogol 300. La composició quantitativa dels excipients no es va poder obtenir de les fitxes tècniques, de manera que desconeixem si la marca comercial o els seus excipients van poder influir en l’aparició de les reaccions. Una limitació important de l’estudi, i que s’ha de tenir en compte per a treballs posteriors, va ser la no realització de proves de provocació a càrrec de el Servei d’Al·lergologia per poder discernir si les reaccions aparegudes van ser provocades pel principi actiu o els excipients.
Finalment, amb els resultats obtinguts en aquest estudi, les mesures que s’han pres en el nostre centre han estat reforçar la premedicació de docetaxel, i realitzar una administració lenta de l’preparat (2-3 hores) en el primer i segon cicle de tractament. Amb paclitaxel es va decidir continuar amb la mateixa metodologia de treball, segons s’indica a la fitxa tècnica.
Conclusions
Docetaxel és el taxano que en el nostre entorn s’ha relacionat amb un major nombre de reaccions adverses durant la seva infusió, superior a les dades descrites a la bibliografia.
Una premedicació adequada tant en hospital de dia com en el domicili de l’pacient, és crucial per reduir la incidència d’aquestes.
És imprescindible realitzar més estudis per poder conèixer amb exactitud l’etiologia d’aquestes reaccions i així poder aplicar mesures efectives que evitin la seva aparició.
Conflicte d’interessos
Els autors declaren no tenir cap conflicte d’interessos.
Bibliografia
1. Fitxa Tècnica Docetaxel (Taxotere®) (accés Juny 2010). Disponible a: www.agemed.es
2. Fitxa Tècnica Paclitaxel (Taxol®) (accés Juny 2010). Disponible a: www.agemed.es
3. Bagnall A-M, Forbes C, Lewis R, Golder S, Kleijnen J. An update of a rapid and systematic review of the effectiveness and cost-effectiveness of the taxanes used in the treatment of advanced breast cancer. The National Institute for Clinical Excellence (NHS Centre for Reviews and Dissemination). University of York, abril 2001 (accés Juny 2010). Disponible a: www.nice.org.Regne Unit / Nicemedia / Live / 11435/32235 / 32235.pdf
4. Gligorov j, lotz j-p. Farmacologia preclínica dels taxanes: implicacions de les diferències. L’oncòleg. 2004; 9 (SUPL 2): 3-8.
5. Hennenfent K L, Govindan R. Formulacions noves de Taxanes: una revisió. Vi vell en una ampolla nova? Anals d’Oncologia. 2006; 17: 735-49.
6. Deu Tije AJ, Verweij J, Loos WJ, Sparboom A. Efectes farmacològics de la formulació de vehicles: Implicacions per a la quimioteràpia del càncer. Clin Farmacokinet. 2003; 42 (7): 665-85.
7. Markman M. Gestió de toxicitats de taxanitat. Càncer de suport a la cura. 2003; 11 (3): 144-47.
8. Actualitzat. Base de dades. Reaccions d’infusió a la quimioteràpia sistèmica; Octubre 2009 (Acceso Marzo 2010). Disponible en: http://www.uptodate.com/contents/infusion-reactions-to-systemicchemotherapy
9. Michaud lb. Mètodes per prevenir les reaccions secundàries a Cremòfor El. Ann Farmachother 1997; 31: 1402-4.
10. Weiss RB, DonedHower RC, Wiernik PH, et al. Reaccions d’hipersensibilitat de Taxol. J Clin Oncol. 1990; 8: 1263-8.
11. Institut Nacional de Càncer Criteris de toxicitat comuns per a esdeveniments adversos (CTCAE) V3.0; Agosto 2006. (Acceso Marzo 2010). Disponible en: http://ctep.cancer.gov/protocolDevelopment/electronic_applications/docs/ctcaev3.pdf
12. Naranjo Ca, Busto U, els venedors, Sandor P, Ruiz I, Roberts Ea, et al. Un mètode per estimar la probabilitat de reaccions adverses farmacèutiques. Clin Farmacol. 1981; 30: 239-45.
13. Sèries d’assistència sanitària de Micromedex. Base de dades de drogues. Sèrie Thomson (Acceso Marzo 2010). Disponible en: www.thomsonhc.com
14. Dizon DS, Schwartz J, Rojan A, Miller J, Pires L, disilvestro p, et al. Sensibilitat creuada entre Paclitaxel i Docetaxel en un programa de càncers femenins. Ginecol oncol. 2006; 100 (1): 149-51.
15. Markman M, Kennedy A, Webster K, et al. Reaccions hipersensibilitat associades a Paclitaxel: experiència del programa d’oncologia ginecològica del Centre de Càncer Cleveland Cleveland. J Clin Oncol. 2000; 18 (1): 102-5.
16. Castells MC, Tennant NM, Sloane de, Ida Hsu F, Barrett Na, Hong Di, et al. Reaccions d’hipersensibilitat a la quimioteràpia: Resultats i seguretat de la desensibilització ràpida en 413 casos. J Allergy Clin Immunol. 2008; 122: 574-80.
17. Feldweg am, Lee CW, Matulonis UA, Castells M. Desensibilització ràpida per a les reaccions d’hipersensibilitat a Paclitaxel i Docetaxel: un nou protocol estàndard utilitzat en 77 tractaments reeixits. Ginecol oncol. 2005; 96: 824-49.
18. Syrigou E, Dannos I, Kottas E, Makrilia N, Tourcantonis I, Dilana K, et al. Reaccions d’hipersensibilitat a docetaxel: avaluació retrospectiva i desenvolupament d’un protocol de desensibilització. Int Arch Allergy Immunol. 2011; 156 (3): 320-4.
19. J Lokich J, Anderson N. Paclitaxel reaccions hipersensibilitat: un paper per a la substitució de Docetaxel. El centre de càncer de Boston. Anals d’Oncologia. 1998; 9: 573-4.
20. Lluna C, Verschraegen CF, Bevers M, Freedman R, Kudelka AP, Kavanagh JJ. Ús de docetaxel (taxotere) en pacients amb hipersensibilitat de Paclitaxel (Taxol). Medicaments anticancers. 2000; 11 (7): 565-8.
21. Bernstein bj. Docetaxel com a alternativa a Paclitaxel després de reaccions d’hipersensibilitat aguda. Ann Farmacher. 2000; 34 (11): 1332-25.
22. Baker J, et al. Efectes secundaris relacionats amb Docetaxel i la seva gestió. Revista Europea d’Infermeria Oncològica. 2009; 13: 49-59.
23. Lee C, Gianos M, Klaustermeyer WB. Diagnòstic i gestió de reaccions d’hipersensibilitat relacionades amb agents de quimioteràpia de càncer comuns. Ann Allergy Asma Immunol. 2009; 102 (3): 179-87.
24. Ardavanis A, TryFonopoulos D, Yiotis I, Gerasimidis G, Baziotis N, Rigatos G. Naturalesa no al·lèrgica de les reaccions d’hiper sensibilitat aguda induïda per docetaxel. Medicaments anticancers. 2004; 15 (6): 581-5.
25. Sánchez-Muñoz A, Mediola Fernández C, Poza Guedes p, Canto Diez G, Bezares Montes S, Cortés Funes H. Hipersensibilidad A Carboplatino i Paclitaxel: Revisión y recomendaciones clínicas. Rev oncol. 2002; 4 (2): 68-71.
26. Cortijo-Cascajares S, Jiménez-Cerezo MJ, Herreros de Tejada A. Revisió de les Realcciones de Hipersensibilidad A Antineoplásicos. Farm Hosp. 2012; 36: 148-58.
27. Chung ch. Gestionar les premedicacions i el risc de reaccions a la teràpia infusional d’anticossos monoclonals. Oncòleg. 2008; 13: 725-32.
28. Markman M, Kennedy A, Webster K, et al. Característiques clíniques de les reaccions d’hipersensibilitat a carbopantain. J Clin Oncol. 1999; 17 (4): 1141-5.