ARTICLES D’INVESTIGACIONS FACULTATIUS DOCENT
Avaluació de tres substrats emprats en la prova d’immunofluorescència indirecta que mesura anticossos antimitocondrials per a diagnòstic de cirrosi biliar primària
POMA Huanca, PATRICIA1 SOSA Tordoya, LUIS FERNANDO1 a CORRESPONDÈNCIA: PATRICIA POMA a AV. SAAVEDRA 2224 (EDIFICI SELADIS, PIS 4). TELÈFON: 2612445
[email protected] de 1 Institut de Servei de Laboratoris de Diagnòstic i Investigació en Salut (SELADIS) -FCFB-UMSA
Resum
la cirrosi biliar primària (CBP) és una malaltia hepàtica inflamatòria crònica d’etiologia desconeguda caracteritzada per la destrucció dels conductes biliars intrahepàtics que desencadena una cirrosi hepàtica. En el present estudi es va avaluar 03:00 substrats comunament emprats per detectar anticossos antimitocondrials (AMA) per Immunofluorescència Indirecta (IFI) per al diagnòstic de CBP. Els substrats avaluats van ser: tall histològic (ronyó de ratolí), cèl·lules Hep-2 (cèl·lules epitelials derivades de l’carcinoma laringi humà) i cèl·lules BHK-21 (fibroblasts de ronyó de hàmster daurat de Síria) dels quals van ser comparats amb els resultats de la prova confirmatòria (assaig inmunoenzimático) comercial que mesura anticossos anti antígens M2 mitocondrials (ELISA, Trinity Biotech).
Es van seleccionar 25 sèrums amb resultats positius per a AMA per ELISA (índex > 1,10UI / ml). Els controls negatius eren sèrums de pacients que no tenien antecedents de malaltia hepàtica i presentaven resultats negatius per a AMA (índex < a 0,90 UI / ml).
dels tres substrats avaluats, els basats en línia cel·lular BHK-21 van mostrar tenir utilitat limitada, amb valors d’eficiència de l’56%, sensibilitat de l’48%, especificitat de l’64% i un índex de concordança de Kappa de 0,12 (baix) pel que fa als resultats de la prova Gold estàndard (ELISA-AMA). Per al substrat Hep-2 es va trobar una concordança moderada (Kappa = 0,6) enfront de l’Gold estàndard, es va obtenir una especificitat = 100%, sensibilitat = 60% i eficiència del 80% Els talls histològics de ronyó de ratolí van mostrar una sensibilitat , especificitat i eficiència de l’92%; a més van mostrar resultats de més concordança amb el mètode d’ELISA (Kappa = 0,84). Dels tres mètodes d’immunofluorescència avaluats es va determinar que el que fa servir talls histològics de ronyó de ratolí és el més eficient i per tant podria ser una eina útil com a mètode tamís en el diagnòstic de CBP.
Paraules clau
Cirrosi Biliar Primària (CBP), Anticossos antimitocondrials (AMA), Immunofluorescència Indirecta (IFI).
Abstract
Primary biliary cirrhosis (PBC) is a chronic inflammatory liver disease of unknown etiology characterized by the destruction of the intrahepatic bile ducts that triggers liver cirrhosis. In the present study we evaluated three commonly used Substrates for mitochondrial antibodies (AMA) by indirect Immunofluorescence (IIF) for the diagnosi of PBC. The Substrates were evaluated: histological (ratolí kidney), Hep-2 cells (Epithelial cells derived from human laryngeal carcinoma) and BHK- 21 (hamster kidney fibroblasts Golden Syrian) which were compared with the results of the confirmatory test (enzyme immunoassay) commercial antigens Measured M2 mitochondrial antibodies (ELISA, Trinity Biotech).
We selected 25 positive serà for AMA by ELISA (index > 1.10 IU / ml). Negative controls serà were from patients who had no history of liver disease and had negative results for AMA (index < 0.90 IU / ml).
Of the three Substrates tested, the based on BHK -21 cell line were shown to have limited usefulness, efficiency values of 56%, sensitivity 48%, specificity of el 64% and Kappa Concordance index of 0.12 (low) MEADE on the results of the Standard Gold Test ( ELISA -AMA). For Hep-2 was moderate agreement (Kappa = 0.6) versus the Gold standard, we Obtained 100% of specificity, sensitivity = 60% and 80% of efficiency. Histological ratolí kidney showed a sensitivity, specificity and efficiency of 92%, results also showed better agreement with the ELISA method (Kappa = 0.84). Of the three methods of Immunofluorescence evaluated it was determined that histological ratolí kidney is the most efficient substrate and therefore could be useful es a screening test for diagnosing of CBP.
Key words
Primary Biliary Cirrhosis (PBC), anti-mitochondrial antibodies (AMA), indirect Immunofluorescence (IIF).
INTRODUCCIÓ
La CBP definida així per Ahrensy Payne el 1950, és una malaltia hepàtica crònica progressivament colestàsica, caracteritzada per la inflamació i destrucció dels conductes biliars interlobulares i septals intervingut per limfòcits T que culmina en una insuficiència hepàtica. S’assumeix que és una malaltia autoimmune causa que comunament va associada a acidosi tubular renal, vitiligen, tiroïditis de Hashimoto, síndrome de Sjögren, fenomen de Raynaud, síndrome de CREST, artritis reumatoide, lupus eritematós sistèmic i deficiència en la funció de limfòcits T supressors. (Zumueta & Navarrete, 2008).
Els seus principals manifestacions clíniques són fatiga, pruïja, icterícia, presència de xantomes, xantelasmes i conseqüències de mala absorció intestinal, com com deficiència de vitamines i osteoporosi (CBP1). La CBP afecta més a dones entre els 30 i 60 anys d’edat, la relació d’afectació home dona és de 9 a 1. També, s’ha determinat que existeix cap genètica amb l’HLA-DR8. (Idrovo, 2007).
Un marcador serològic característic de la malaltia és la presència d’AMA, sent el blanc antigènic la proteïna M2 de la membrana interna del mitocondri (component E2 de la piruvat deshidrogenasa), altres proteïnes antigèniques mitocondrials com M4, M8 i M9 estan involucrades en menor proporció. Els AMA es troben presents en el 90% dels pacients amb CBP, i en el 30% dels casos poden estar acompanyats per patró fluorescent citoplasmàtic i / o patró perifèric en la prova d’anticossos antinuclears. (Bruguera & Ichiyanagui, 2008). Els AMA en menor freqüència, també poden trobar-se en malalties hepàtiques induïdes per drogues, sífilis, tuberculosi i altres malalties autoimmunes hepàtiques. (O’Brien, Jordan, Guindi, Hans & Dienes, 2009).
El diagnòstic serològic de CBP es basa en IFI i ELISA. La IFI fa servir com a substrat talls histològics de fetge, ronyó o estómac de ratolí o rata i la línia cel·lular Hep-2. Els tests d’ELISA fan servir com a substrat antígens de l’complex piruvat deshidrogenasa obtingut de cor boví o porcí (Dahnrich, Pares, Llorenq Cavalleria, Wolfgang & Probst, 2009).
Un avantatge característica de la prova d’IFI és que permet avaluar a el mateix temps diversos tipus de proteïnes antigèniques en un mateix substrat (Exemples: SP100, Gp210, LB2, LKM1, LC1, SLA, M1 – M9) el que la fa una prova molt sensible, en canvi la prova d’ELISA utilitza antígens purificats per a un sol marcador de laboratori el que li dóna característica de major especificitat. En el test d’ELISA una mostra que contingui anticossos d’alta afinitat en baixa concentració, pot presentar la mateixa densitat òptica que una mostra amb anticossos de baixa afinitat però amb alta concentració per tant no proporciona informació quantitativa com passa amb la tècnica de IFI, en què és possible determinar mitjançant una sèrie de dilucions el màxim títol d’anticossos presents a la mostra d’un determinat pacient (Cortés & Mancera, 2009).
entre els anys 2008 i 2009, al laboratori d’Histocompatibilitat i Inmunogenética de l’Institut SELADIS, s’ha observar que van existir 162 sol·licituds de determinació d’AMA, de les 162, 49 van donar reactives per AMA. Per fer un bon diagnòstic i seguiment d’aquest tipus de malaltia es requereix de mètodes de diagnòstic comercials o optimitzats i validats d’alta sensibilitat i especificitat diagnòstica. El coneixement d’aquests aspectes fa que hi hagi la garantia que el diagnòstic de laboratori per un determinat mètode sigui eficient i fiable. Per abans esmentat, en el present treball s’avaluen 3 substrats (talls histològics de ronyó de ratolí, línia cèl·lules Hep-2 i línia cel·lular BHK-21) de la prova d’IFI per al diagnòstic de CBP que mesura AMA per tal de determinar com substrat és el més sensible, específic, eficient i que té millor concordança amb la prova d’ELISA que mesura AMA.
MATERIALS i MÈTODES
Població en estudi
Les mostres utilitzades en aquest estudi provenien de pacients que van assistir a l’institut SELADIS durant abril de 2008 a maig de 2009. Les mostres de panell de sèrums positius provenien de pacients amb diagnòstic clínic de CBP amb serologia negativa per hepatitis virals i que havien donat resultats d’ELISA (Trinity Biotech) per AMA positius (índex de la mostra > 1,10 UI / ml). Les mostres de el panell de sèrums negatius eren sèrums de pacients aparentment sans sense antecedents de malaltia hepàtica (resultats de transaminases, fosfatasa alcalina i bilirrubines normals, serologia per virus d’hepatitis negativa i resultats d’ELISA per AMA negatiu (índex < 0,90 UI / ml).Cadascun dels panells de sèrums estaven constituïts per 25 mostres. Tots els pacients dels que es va utilitzar els sèrums per construir els panells de sèrums positius i negatius van donar el seu consentiment perquè la seva mostra sigui utilitzada en el present estudi.
Anàlisi de dades
Tots les dades de el present estudi van ser realitzats amb ajuda de la base de dades Excel 2007, es van utilitzar els indicadors estadístics per validacions com l’índex de Kappa i la prova de Mac Nemar (López de Ullibarri & Cura, 2008).
Preparació d’empremtes
empremtes amb el substrat de cèl·lules BHK- 21
Tot aquest procediment es va dur a terme en campana de flux laminar (Gelaire) i es va treballar amb material nou i estèril.
es va descongelar 1 alíquota de cèl·lules guardades en nitrogen líquid i d’aquest es va transvasar a un tub falcon de 15 ml i es va afegir 3 ml de RPMI 1640 després es va centrifugar a 2500 rpm per 5 min, complert aquest temps es va eliminar el sobrenedant i es resuspendió el pèl·let l’1 ml de RPMI 1640 s uplementado (10% de Suero Fetal Bobino (SFB) suplementat, antibiòtics (gentamicina i estreptomicina), després es va transferir a una caixa de cultiu cel·lular de 25 cm2 i es va incubar durant una setmana a 37 ° C, 5% C02 i 90% humitat relativa.
Una vegada que la placa es trobava en confluència es vercenizó durant 10 min a 37 ° C perquè es desprenguin totes les cèl·lules les cèl·lules adherides a la base de la caixa de cultiu, les cèl·lules vegada desenganxades es van col·locar en tub falcon de 15 ml i es centrifugar a 1500 rpm per 5 min. Es va eliminar el sobrenedant, es resuspendió el pèl·let en 1 ml d’RPMI1640 suplementat i es va ajustar la concentració cel·lular a 2,5×106 cèl·lules / ml. En portaobjectes de 12 pous (MP Biomedicals, USA) es van preparar empremtes col·locant 8 uL de les cèl·lules ajustades a cada vaset. Es va centrifugar les empremtes a 1000 rpm per 3 min i es van embolicar les empremtes amb parafilm (3M), per a la conservació de les mateixes es van dur a 4 ° C per 30 min i després es van conservar a -20 ° C fins a la seva utilització.
Empremtes amb el substrat talls histològics de ronyó de ratolí
Es va extreure ronyons de 25 ratolins (Swiss albins) de 28 setmanes amb pes mitjana de 20 g +/- 2 g, dels quals van ser donats pel Bioterio de la Facultat de Ciències Farmacèutiques i Bioquímiques. Es va rentar els ronyons amb buffer salí de fosfats (PBS) constituït de Fosfat de sodi 112,5 mmol / L, fosfat de potassi 30mmol / L, clorur sòdic 1,15 mol / L, azida de sodi 0,95 g / L pH 7,5. Després, els ronyons es van col·locar en una caixa Petri que contenia carboximetil cel·lulosa de sodi (Sigma Aldrich) a el 4% i es va dur a congelació a -20 ° C fins al moment de la seva utilització. Per realitzar els talls criostáticos es van preparar tacs amb els ronyons embassats en carboximetil cel·lulosa de sodi a el 4%. Els talls es van realitzar a congelació utilitzant un criostat (LEYCA) a -27 ° C, es va col·locar quatre corts de ronyó per cada làmina de portaobjectes. Els talls realitzats tenien diàmetre mitjana de 5 mm i 5 um de gruix.
Preparació de l’conjugat fluorescent
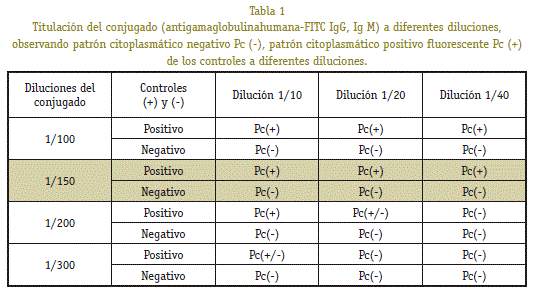
Per a determinar el títol òptim de l’conjugat fluorescent (anti gammaglobulina humana IgG i IgM marcada amb tioisocianato de fluoresceïna) es van preparar les dilucions (1/100, 1/150, 1/200 i 1/300) amb dil | úyete de l’conjugat (50 uL de blau d’Evans 0,4% en 3,5 ml de PBS) .
titulació de l’conjugat fluorescent per a la prova de “IFI que fa servir com a substrat talls histològics de ronyó de ratolí i línia cèl·lules BHK-21.
per a la titulació de l’conjugat fluorescent es va utilitzar controls positius i negatius per a AMA provinents de la casa comercial Orgentec, Alemanya.
es van fixar les empremtes amb acetona pa freda (-20 ° C) per 8 min, es hidrataron per 10 min en una gerra Koplin contenint PBS (10x) pH 7,2. es van realitzar dilucions (1 / 10,1 / 20 i 1/40) dels sèrums control positiu i negatiu. Després, es va sembrar 40 uL de les dilucions de sèrums , Es va incubar per 30 min a temperatura ambient (T ° A) i en càmera humida per evitar la dessecació dels talls histològics o de les cèl·lules fixades. Es van rentar les empremtes per 10 min en PBS i en agitació contínua. Les empremtes van ser assecades amb paper absorbent i van ser col·locades novament en càmera humida. Es va col·locar 25 uL de les dilucions a avaluar de l’conjugat fluorescent (1 / 100,1 / 150, 1/200 i 1/300). Es va incubar en foscor per 30 min aT ° A. Complert aquest temps, es va realitzar el procés de rentat i assecat abans descrit. Es va agregar la solució de muntatge (Mowiol 12%, Glicerol 30%, Tris 20 mmol / L, azida de sodi 0,95 g / L) i es va col·locar un cobreobjectes sobre cada portaobjeto per evitar la dessecació de les empremtes. Finalment es van llegir les plaques en microscopi UV amb augment 40X.
Immunofluorescència indirecta (IFI)
La prova d’IFI amb cèl·lules Hep-2, es va realitzar segons les instruccions de fabricant de el kit comercial (The Binding Site, UK).Breument: es van realitzar dilucions 1 / 40,1 / 80 i 1/160 dels panells de sèrums i de sèrums controls.
Es va incubar 30 minuts a T ° A. Es van rentar per 10 min i van assecar les plaques corresponents, es va afegir conjugat i va incubar en foscor per 30 minuts, després es van rentar i assecar novament les empremtes i es va col·locar el mitjà de muntatge. Les plaques en microscopi UV amb augment 40X.
Per a la realització de les proves d’IFI amb cèl·lules BHK-21 i talls histològics es va seguir el protocol descrit en la titulació de l’conjugat, amb l’excepció que es va utilitzar el títol òptim de l’conjugat per a cada substrat. Amb tots els substrats avaluats es va utilitzar simultàniament un control positiu i negatiu (Orgentec). El control positiu d’AMA havia de produir un patró citoplasmàtic color verd poma amb intensitat (++) des de la dilució 1/40. El control negatiu no havia d’emetre fluorescència a la dilució 1/10 en les cèl·lules renals o 1/40 en les línies cel·lulars. (Binding Site, 2011).
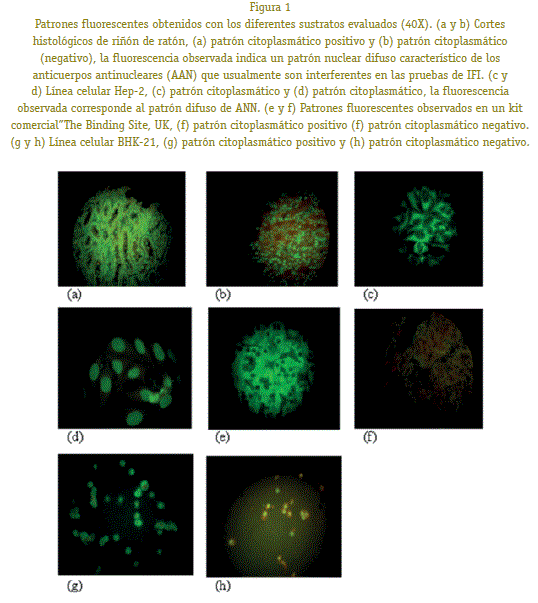
Per interpretació de resultats de les proves d’IFI, es van considerar mostres negatives quan existia absència de fluorescència verd poma a citoplasma. Una mostra va ser considerada positiva si la coloració de l’citoplasma era més gran a l’control negatiu. (Fig. 1).
Per a fins de l’estudi es va considerar com a estàndard d’or a el Kit d’ELISA que mesura anticossos contra l’antigen M2 mitocondrial marca Trinity Biotech, el qual reporta una sensibilitat 91% de i especificitat de 100%. (Jones & Metcalf, 2008).
RESULTATS
A l’fer l’anàlisi prèvia dels pacients que assistien a el servei de laboratori es va determinar que de totes les proves sol·licitades per a la detecció de malalties autoimmunes durant dues gestions (2008 i 2009) es sol·licitava la determinació d’AMA (ELISA) un 7% dels casos, sent 69 sol·licituds el 2008 i 93 el 2009, tenint un total de 162 casos presumptius de Cirrosi Biliar Primària en les dues gestions. De les 162 mostres 49 van ser conformades com reactives per AMA. Es va observar que la majoria dels pacients diagnosticats com AMA reactius eren dones (80%). Al tauler de sèrums positius es van contemplar sèrums de 20 dones i 5 homes. La mitjana d’edat dels pacients les mostres van ser incloses en el present estudi era de 46 anys, amb valors extrems de 22 i 77 anys.
En el procés de titulació es van realitzar dilucions: 1/10, 1 / 20 i 1/40 dels controls positius i negativos.Luego es va avaluar el títol òptim a el qual podia ser utilitzat el conjugat. Es va avaluar a dilucions de 1/100, 1/150, 1/200 i 1/300. Aquest experiment es va fer per triplicat i com a resultat es va observar que a la dilució 1/150 s’obtenien resultats Veritables Positius (VP) i Veritables Negatius (VN) dels sèrums controls comercials.
Avaluació dels resultats de el test diagnòstic en els tres substrats avaluats
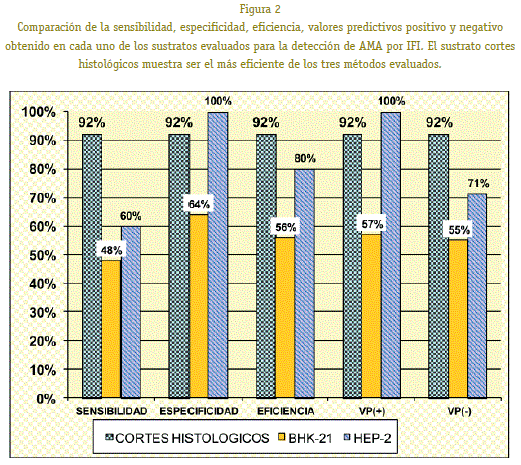
a l’avaluar a l’sensibilitat, especificitat, valors predictius positius i negatius i l’eficiència dels tres substrats avaluats es va observar que la línia cel·lular BHK-21 és el substrat menys eficient, el substrat cèl·lules Hep-2 va mostrar tenir major especificitat, menor sensibilitat i per tant menor eficiència que el substrat talls histològics. Els resultats clarament mostren que el substrat talls histològics és el mètode més eficient per al diagnòstic per IFI per CBP.
Determinació de concordances de diferents substrats emprats per AMA IFI enfront resultats trobats per ELISA
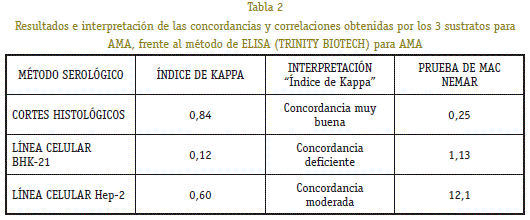
Les proves de concordança utilitzades van ser: Índex de Kappa i la Prova de Mc Nemar per a dues proves relacionades (aparellades). Els resultats de les diferents proves de concordança (p < 0,05) per als diferents substrats versus el mètode d’ELISA que mesura anticossos anti antigen M2 mitocondrial (Gold Standard). El valor crític esperat en el test de Mc Nemar era de 3,84 (p < 0,05).
Els talls histològics van mostrar un índex Kappa de 0 , 84 que segons l’escala de l’índex correspon a una concordança molt bona amb els resultats obtinguts pel mètode d’ELISA. La prova de Mc Nemar presentar un resultat de 0,25.
La línia celularBHK-21 va presentar un índex Kappa de 0,12 (concordança deficient) amb els resultats obtinguts pel mètode d’ELISA. La prova de Mc Nemar va mostrar va mostrar un valor de 1,13.
La línia cel·lular Hep-2 va presentar un índex de kappa de 0,6 (concordança moderada) enfront dels resultats obtinguts pel mètode d’ELISA . El valor de Mc Nemar va ser de 12,1.
A causa que els talls histològics van mostrar ser el fico de IFI més eficient per al diagnòstic de CBP per IFI, es van comparar els resultats davant un mètode comercial de IFI per AMA.L’índex Kappa trobat va ser de 0,66 (concordança molt bona). La prova de Mc Nemar va presentar un valor de 1,33.
DISCUSSIÓ
A l’analitzar els casos positius per CBP en el nostre laboratori, vam determinar que el 80% dels casos afecta dones , sent la relació dona / home 4: 1 aquestes troballes són similars als reportats per: Abarca, Penya Herrera & Garces (2006) on determinen la Etiologia, supervivència, complicacions i mortalitat en cirrosi hepàtica en l’Equador evidenciant una relació dona / home de 2,4: 1; també Cedeño & Medina (2008) determinen que el 90% de les dones són afectades per aquesta malaltia. De les 25 mostres positives que es van emprar en aquest estudi 20 provenien de dones. Valera, Smok & Poniachik (2007) en l’estudi que van realitzar a l’Hospital Clínic de la Universitat de Xile ia la Clínica les Comtes de Xile en 115 pacients, van mostrar que 110 eren dones el que equivalia a l’96% trobant una relació d’afectació dona / home de 9: 1, es coneix que els factors hormonals són un dels factors que predisposen a malalties autoimmunes. (Rojas, 2007, pàg. 324).
En el present estudi vam determinar que l’edat en què es presenten majorment casos d’CBP és de 45 anys. Dades similars van ser reportats per Dávalo, Román & Bustios (2007) en un estudi d’Hepatitis autoimmune en el qual incloïen a la CBP mes les seves formes clíniques i factors relacionats amb la resposta a l’tractament mostrant rang d’edats d’afectació freqüents des de 48 a 59 anys, una possible explicació a aquest fenomen és que a aquesta edat l’estafa ha perdut en gran part la seva capacitat per destruir per selecció negativa als limfòcits T autoreactius, la qual cosa és un factor predisponerte a malaltia autoimmune.
Fer un bon diagnòstic clínic i laboratorial per a aquest i altres tipus de malalties autoimmunes és vital, principalment a causa de l’caràcter invalidant en el pacient o a el fet que puguin posar en risc la vida de l’pacient en altres casos. En aquest últim aspecte Jones & Metcalf (2008) van determinar que els pacients amb CBP en estadi III / IVDE la malaltia tenen major mortalitat (43.6%) que la població normal. Per tant, en cas d’un diagnòstic laboratorial de CBP s’ha de comptar amb una prova de major eficiència possible. En la nostra experiència observem que utilitzant substrats ja siguin, línies cel·lulars (BHK- 21, Hep-2) o talls criostáticos de teixits (fetge o ronyó de ratolí) es pot evidenciar fluorescència a nivell de citoplasma cel·lular la qual cosa està directament relacionada a malalties hepàtiques de tipus immunològic, infeccions virals o altres autoimmunes extra he Paticas, etc. (Almeida et al., 2008).
Dels tres substrats avaluats vam determinar que els basats en línies cel·lulars tenen utilitat limitada, especialment els que utilitzen la línia cel·lular BHK-21 que tenen una eficiència de l’56%, sensibilitat de l’48% i especificitat de 64%. Si bé aquest substrat és considerat bo per determinar anticossos antinuclears. (Sosa & Sánchez, 2007) no ho és per al diagnòstic de CBP ja que té una concordança baixa amb la prova Gold estàndard avaluada (ELISA-AMA). No hi ha reportis en la bibliografia sobre la presència o absència d’aquests antígens mitocondrials en la línia cel·lular BHK-21.
Una troballa interessant va ser trobar que amb la línia cel·lular Hep-2 tot i tenir una concordança moderada (segons índex Kappa) enfront de el test d’ELISA, va mostrar tenir una especificitat de l’100%, val a dir que si s’utilitzés aquest substrat no s’observés fluorescència a nivell de citoplasma cel·lular, es podria dir que el pacient no presenta la malaltia però tot i així , cal utilitzar una prova més eficient per confirmar l’abans esmentat. Pel que fa a la sensibilitat d’aquest substrat no s’observa una diferència significativa amb les cèl·lules BHK-21.
Els talls criostáticos de ronyó de ratolí van mostrar ser els més eficients amb 92% de sensibilitat i especificitat de l’92% respectivament. A més van mostrar emetre resultats de més concordança amb el mètode d’ELISA-AMA (Kappa 0.84). En general es coneix que la sensibilitat i especificitat dels mètodes de IFI per AMA són de l’95% (Valera, Smok & posava-chik, 2007). Aquests resultats ens mostren que el mètode IFI optimitzat al laboratori d’Histocompatibilitat i Inmunogenética de l’Institut SELADIS és tan bo com els mètodes similars oferts per les diferents cases comercials.Si bé hi ha diferències a nivell de sensibilitat i l’especificitat amb el mètode d’ELISA (mètode definitiu per diagnosticar CBP), l’única o potser la més important avantatge que té el mètode de IFI enfront de el de el mètode d’ELISA és que no només es limita a detectar l’antigen M-2 mitocondrial, sinó que pot donar resultats positius contra els antígens M1 a l’M9. Orientant d’aquesta manera a el metge cap al diagnòstic de malalties hepàtiques autoimmunes, tipus I, II, III o altres autoimmunes no hepàtiques i fins i tot casos d’infeccions virals. (Meléndez & Dujarric, 2008). Un altre avantatge no menys important és, que el mètode optimitzat fa més accessible la prova als pacients a causa de que el cost de reactiu per prova és de Bs. 13 enfront de Bs. 45 de l’Kit de immunofluorescència i Bs. 31,50 de l’Kit d’ELISA. El mètode optimitzat també mostra desavantatges, la primera és el consum de temps (sacrificar el ratolí, extracció i conservació dels ri-senars, les dilucions seriades de mostres controls, els rentats, la lectura en el microscopi de fluorescència). Per l’experiència pròpia, trobem que s’inverteix d’una hora a una hora i mitja més processant les mostres per IFI que per ELISA. A més és important recalcar que es necessita professionals capacitats per fer la lectura i interpretació dels patrons fluorescents. Una altra troballa important trobat va ser que es va poder evidenciar diferents patrons citoplasmàtics fluorescents en un determinat substrat. Amb els resultats obtinguts de el present estudi es va aconseguir determinar que dels tres substrats avaluats, els talls histològics de ronyó de ratolí són el substrat més eficient i és el substrat que té millor concordança amb els resultats de la prova d’ELISA per al diagnòstic de CBP . D’altra banda, es va determinar que hi ha una concordança molt bona amb els resultats de IFI d’un kit comercial de similars característiques. El test diagnòstic emprat ens ha permès validar el test d’IFI que fa servir talls histològics com una prova tamís per al diagnòstic de CBP.
REFERÈNCIES
Eduard, Z., Villena, J. , Navarrete, S., & Figueroa. (2008) .Cirrosis Biliar Primària Relació Clínic-Laboratorial i Patològica. Malalties de l’Aparell Digestiu 1 (4), 5-8.Recuperado de http://www.cfnavarra.es/salud/anales/textos/vol26/n3/revis2a.html
Bruguera, M. (2009). Diagnòstic i tractament. Malalties de les vies biliars intrahepàtiques distals en l’adult: colangitis i ductopenia.Med Clin (Barcelona), 1 07,338 341. Recuperat de http://www.donostiaospitalea.orgcats/cats61.htm
Idrovo, C. (2007). Cirrosi Biliar Primaria.Tratamiento. Bogotà. Fundació Santa Fe. Madrid: Elsevier
Ichiyanagui, C., & Rodriguez,. (2008). Malalties hepàtiques colestàsiques. Departament de Malalties de l’Aparell Digestiu. 1 (4). Recuperat de http://www.cfnavarra.es/salud/anales/textos/vol26/n3/revis2a.html.
Brien, C., Jordan, J., Maha, G., Hans, P., Dienes, J., & Heathcot, L. (2009 ) Term Follow-Up of Ant mitochondrial Antibody-Positive autoimmune Hepatitis Hepatologi 48 (2), 550-556. Recuperat de http://onlinelibrary.wiley.com/doi/10.1002/hep.22380/pdf
Dahnrich, C., Pares, A., Llorenç, C., Rosemann, A., Wolfgang, S., & Vergani, D. (2009). Detecting Primary Biliary Cirrhosis-Specific Antimitochondrial Antibodies. Clinical Chemistry Stocker, 55: 5,978-985, Recuperat de http://www.biomedexperts.com/Profile.bme/1655595/dimitrios_bogdanos
Cortés, L., & Mancera, L. (2008). Concordança entre ELISA i IFI per a la determinació d’anticossos tipus IgG contra Toxoplasma gondii. Associació Colombiana d’Infectología. Recuperat de http://www.aeped.es/protocolos/infectologia/index.htm
Ullibarri, L. (2008). Mesures de concordança: l’índex de Kappa The design and anàlisi of clinical experiments Galparsoro 6,169-171. Recuperat de http://www.fisterra.com/mbe/investiga/kappa/kappa2.pdf
Cura, I. (2004). Manual de procediments de control de qualitat per als Laboratoris de Serologia dels Bancs de Sang. Washingtong, D.C: Organització Panamericana de la Salut.
Binding Site. HEp-2 ANA / Substrate Slides. Insert de l’Kit commercial.
Trinity biotech. CaptiaTM mitocondri Insert de l’Kit comercial. Jones, D., & Metcal. (2008). Pronòstic de la Cirrosi Biliar Primària. Hepatologi 26,1138-1.142. Recuperat de http://www.donostiaospitalea.org//cats/cats61.htm
Abarca, J., Peñaherrera, V., & Garces, C. (2006) . Etiologia, supervivència, complicacions i mortalitat en cirrosi hepàtica en l’Equador. Avaluació retrospectiva de 15 anys En Latinoamerica 1,29-34.
Cedeño, L., & Medina, J. (2008). Cirrosi Biliar Primària. Medisan. Recuperat de http://74.125.47.132/search?q=cache:xSGNf_1n07MJ:bvs.sld.cu/revistas/san/vol11_307/san12307.htm cirrosi biliar primària en dones.
Valera, J.M., Smok G., & Poniachik, G. (2008). Cirrosi biliar primària: experiència de tretze anys en dos centres de referència.Rev Méd Xile 4,469-474. Recuperat de http://www.scielo.cl/scielo.php?pid=S003498872006000400010&script=sci_arttext
Rojas, W. (2004). Immunologia. 13aed. Medellin Colombia.Corporación per a investigacions Biològiques p 324.
Dávalo, M., Román, R., & Bustios, C. (2008). Hepatitis autoimmune: Formes clíniques i factors relacionats amb la resposta a el tractament. Gastroenterol. 24: 305-313. Recuperat de http://www.cfnavarra.es/salud/anales/textos/vol26/n3/revis2a.html.
Almeida, J. (2002). Anticossos antiribosomales com a marcadors d’activitat en el LES. Annals de Medicina Interna. Madrid.
Porcel, J. (2007). Proves de laboratori per a l’estudi de les malalties sistèmiques autoimmunes. Clínica-UNR.org, Recuperat de http://www.clinica-unr.org/Especiales/20/Especiales%20Laboratorio_Porcel.pdf
Harrison, (2007). Criteris Diagnòstics D’Hepatitis Autoimmune. Manual of. Medical Therapeutics.
Sosa, L.F., & Sanchez, L. (2004). Validació de mètodes serològics que s’empren per al diagnòstic de malalties reumàtiques definides: Lupus eritematós sistèmic (LES). Biofarbo. 12, 15-19.
Meléndez, M., & Dujarric, M. (2008). Avaluació de la Inmunohistoquímica per al Diagnòstic de les Malalties Autoinmunes.Rev Cubana Invest Biomed 23 (3): 133-8 Recuperat de http://bvs.sld.cu/revistas/ibi/vol23_3_04/ibi01304.pdf.