Note méthodologique
application de modèles structurels marginaux pour estimer les effets de Thérapie antirétrovirale dans 5 cohortes de Seroconverters Virus de l’immunodéficience humaine
Modèles de structure marginaux Application aux effets de la thérapie antirétrovirale dans 5 cohortes de Seroconverters VIH
Santiago Pérez -Thoyosa, B; Ferrerosy Immaculée, C; Miguel A. Hernand; Gemese
École de santé valencienne (EVES), Valence, Espagne;
BDePartaent d’Infermeria Communauté, Médecine préventive Je salut Public I Història de la science, Université d’Alacant, Alacant, Espagne;
École de santé valencienne (EVES), Valence, Espagne; Département de la santé publique, Université Miguel Hernández, Alacant, Espagne;
CDPpar Regamento Santé publique, Universidad Miguel Hernández, Alacant, Espagne;
DDEPARTY DE L’EPIDÉMIOLOGIE, ÉCOLE DE SANTÉ PUBLIQUE, UNIVERSITÉ DE HARVARD, BOSTON, États-Unis;
EGROUP de l’étude multicentrique espagnol des Seroconverters (voir la relation complète de ses membres à l’annexe)
Ce travail a été financé grâce à l’aide à la recherche FIPSE (Fondation pour la recherche et la prévention du sida en Espagne) Intégré par le ministère de la Santé, Abbott Laboratories, Boehringer Ingelheim, Bristol Myers Squibb, Glaxosmithkline, Merck Sharp et Dohme et Roche), (FIPSE 36349/02) et partiellement au FIS (Fonds de recherche sur la santé) (FIS 02/0639) et Aide de l’École de santé valencienne (EVES) 2005.
Gestion de la correspondance
Résumé
Objectifs: Méthodes classiques ont des limites à ajuster par temps dépendant du temps Facteurs de confusion pour évaluer l’efficacité de la population des traitements dans des études d’observation. Dans ce travail, un nouveau type de méthodologie est montré, les modèles structurels marginaux (MEM) et l’efficacité de la thérapie antirétrovirale de grande activité (TARGA) sur l’incidence du sida ou de la mort sont estimés.
Sujets et méthodes: Les sujets ont été identifiés sans Targa suivi de 1997 sur les cohortes de Seroconverters au virus de l’immunodéficience humaine (VIH) du projet Gemes (Multicenter Seroconverter Seroconverter). Pour estimer l’effet sur l’incidence du sida ou de la mort, les paramètres d’un MEM ont été obtenus grâce à une régression logistique pondérée pour une probabilité inverse. L’estimation des poids était basée sur le nombre de CD4, du temps de la séroconversion, du sexe, de l’âge, de la catégorie de transmission et du traitement antérieur. Résultats: Les 917 sujets éligibles ont été suivis pour une moyenne de 3,4 ans, au cours de laquelle 139 résultats d’intérêt ont été observés. 42,1% des participants ont reçu Targa lors de l’étude. Le taux relatif était de 1,01 (intervalle de confiance (IC) de 95%, 0,68-1,49) au moyen d’un modèle classique non covariable COX, et de 0,90 (95% CI, 0,61 -1,32) à l’aide d’un classique Modèle Cox avec des covariables changeantes au fil du temps. Le taux de causalité relative estimé par un MEM était de 0,74 (CI 95%, 0,49-1.12).
Conclusions: L’effet bénéfique de Targa trouvé par MEM est bien établi, mais les modèles conventionnels ne pouvaient pas le détecter. L’utilisation d’un MEM a permis de régler correctement la variable CD4, qui est à la fois une variable de confusion dépendante du temps et est affectée par l’utilisation précédente du traitement.
Mots-clés: modèles structurels marginaux. Analyse de survie. Efficacité des traitements. SIDA.
Résumé
Objectifs: Méthodes standard pour évaluer l’efficacité de la population des traitements dans des études d’observation ont des limites importantes à AppOodyey Ajuster pour des confeaurs dépendants du temps. Dans cet article, nous décrivons une approche méthodologique récemment développée, des modèles structurels marginaux (MSM) et l’utilisent pour efficacité de l’efficacité de la thérapie antirétrovirale très active (HAART) sur le sida ou l’incendie de la mort.
Sujets et méthodes: Nous avons analysé tous les sujets suivis après 1997 dans le cadre du projet Gemes (acheté par plusieurs cohortes de Seroconverters VIH en Espagne) et qui n’avaient pas utilisé Haart avant le début du suivi. Pour estimer l’effet de HAART sur le sida ou l’incidence de la mort, nous avons estimé les paramètres d’un modèle de Cox structurel marginal en ajustant un modèle de régression logistique pondéré de probabilité inverse. L’estimation des poids était basée sur le nombre de CD4, le temps depuis la séroconversion, le sexe, l’âge, la catégorie de transmission et le traitement précédent. Résultats: 917 sujets éligibles ont été suivis pour une moyenne de 3,4 ans et nous avons observé 139 événements. 42,1% des participants ont reçu Hart pendant l’étude.Le rapport de taux estimé était de 1,01 (intervalle de confiance de 95% (CI), 0,68-1.49) à l’aide d’un modèle COX sans covariables et de 0,90 (95% CI, 0,61-1.32) à l’aide d’un modèle COX avec des covariables dépendant du temps. Le rapport de taux de causalité estimé pour MSM était de 0,74, (95% CI, 0,49-1.12). Conclusions: L’effet bénéfique de HAART estimé par le MSM, mais largement manqué par les méthodes conventionnelles, est conforme aux conclusions d’études randomisées antérieures. Le MSM ajusté de manière appropriée pour le nombre de CD4 de CD4 dépendants dépendant du temps, qui est à la fois un confort variant du temps et est affecté par un traitement préalable.
Mots clés: modèles structurels marginaux. Analyse de survie. Efficacité du traitement. LE SIDA.
Introducción
La Llamada Terapia Antirrettroviral de Gran Actividad (Targa) Combina Al Menos 3 Fármacos, Genermentee Nations Unhibidor de la Proteasa (IP) O INHIHHIBO NUCLEÓSIDO DE LA TransRANCRANSA INVERSA (NNRTI) Junto Con 2 inhibe Nucleósidos de la Transcriptasa Inversa (NRTI). Dos Ensayos CLÍNICOS HAN MOSTRADO QUE LA TARGA, COMPARADA CONDUMEN COMPUESTO POR 2 NRTI1,2, Réduit La Incidencia de Sida Y Muerte Entre Las Personas Infectadas Par El Virus de la Inmunodeficiacia Humana (VIH). Sin Embargo, Los Rulsados de Estos Ensayos CLÍNICOS DE CORTA DURACIÓN (Menos de Nations Año) Aucun permis d’accueil Evaluar La Eficacia A Largo Plazo de la Targa, Una Terapia que Debe Ser Tomada de Por Vida. Par Ello, SE Precisan Estudios Observacionales Longitudinales Para Estimation El Efecto de la Targa A Différentes Estrategias Terapétiticas3-6.
Sin Embargo, La Aplicación de Métodos Estadísticos Convénionales Para Estudios Longitudinales (p. EJ ., Regresión de Cox con Variables Cambiantes en el Tiempo) Puée Proporcionar Etreprades Sesgados del Efecto Causal Del Tratamiento7-10. Este Sesgo Aparece Cuando Hay Facteurs de Riesgo del Evento que Cambien Con El Tiempo, Son Predicts de Del Inicio del Tratamiento, Y Su Valor Está Afecttado por El Uso Previo de Tratamiento. EN ESTUDIOS DE TARGA Y SIDA, UN BAJO RECUENTO DE CD4 ES UNA INDICACIÓN DE INIICIO DE TRATAMIENTO QUE SE Asocia Conf Una Menor Supervivencia (es décirage, es UNA Variable de Confinión dépendante Del Tiempo); Además, El Recuento de CD4 Está Afecttado Par El Inicio del Tratamiento. EL SESGO DE LOS MÉTODOS CONVENCIONES APARÈCE AUN EN AUSENCIA DE CONFUSIÓN DEFUSIÓN INFLUSO SE HUBIERAN MEDIDO TODAS LAS INDLIERANES DEL TRATAMIENTO) Porque SE Debe A Nations Ajuste InaPropado de la Confinión Creada Por Variables Dépendances Por el Tiempo Afectadas Previo.
Descririmos Un Nuevo Tipo de métodología, Los Modelos Estructuries Marginales (MEM), Para Ajustar ApropiaDamente Por Variables de Confinión Dépendances Del Tiempo Afectados Por el Tratamiento Previo. Los Parámetros de Estos Modelos SE ESSTAN Mediante Ponderación Por PondaBilidad Inversa. El Artículo Muestra Una Aplicación Práctica de los Mem Para Estimière La Efectividad de Targa Sobre la Incidencia de Sida.
SUJETOS Y MÉTODOS
DATOS
SE HA UTILIZADO INFORMIÓN Proveniente de las 5 Cohortes de Seroconvertores Al Vih del Proyecto Gemes (Grupo de Estudio MultiCéntrico Español de Seroconvertores) Que HemosCrito Contacte Détaille Contail A Anterioridad11. Para Este Análisis SE Eligió A LOS 917 SUJETOS QUE EN ELLETOS QUE EN ELENTE DE 1997, OF EN EL MOMENTO DE SU INCLUSIÓN EN LA COHORTE SI ESTA HABÍA OCURRIDO CONOSTERIORDAD, Aucun Targa de Recibido Había. Las Siguientes Variables SE Midieron Al Inicio del Seguimiento: Sexo, Edad, Uso Previo de Terapia Antirrettroviral (Pas de targa), Tiempo Desde La Seroconversión Al Vih, Categoría de Transmisión (Hombres Que Mantienen Relaciones Sexuelles Congêtres, Usuarios de Drogas Por Vía Parentéral, Hétérosexuels, OTROS), CD4 Y Carga viral. El Seguimiento SE Organesó En Intervalos Mensuaux Y A Cada Intervalo SE Le Asignó La Medición Más Reciente de CD4 Y Carga Viral. El CD4 SE Clasificó FR 5 GUPOS CONNES SIGUIENTES PUNTOS DE CORTE (50, 100, 200, 350 CÉLULAS / μL). La Carga Viral SE Recodificó de Acuerdo Continualité Puntos de Corte Habituels (400, 1.000, 10.000, 100.000 Copias por ml). La variable Carga virale NO SE USO EN NUESTRO ANÁLISIS PRINCIPAL Porque Aucun ESTÁ DISPONIBLE PARA TODOS LOS INDUSTUOS. El Uso de Targa SE Resumió en Una Variable Dicotómica Con Valor 0 Para Los Meses Previos Al Inicio del Tratamiento, Y 1 para Los Meses Desde el Inicio de Tratamiento Hasta El Final Del Seguimiento. Par Tanto, Nuestro Análisis ES Por Intención de Tratar, es décirage, SE Asmé que cuando Un Paciente Inicia Targa Permanece Siempre en Ella. SE Analizó El Tiempo Desde el Inicio del Seguimiento Hasta El Primero de los Siguientes Eventos: El Diagnóstico de Sida O Muerte, La Périda de Seguimiento, Optième de 2004.
Modèles de structure marginaux
L’objectif de notre analyse est de comparer le taux d’incidence du sida / décès qui aurait été observé, si toutes les personnes avaient initié Taga au début du suivi. , avec le taux d’incidence sur le sida / décès qui aurait été observé si aucun patient n’avait initié Taga lors du suivi. Chacun de ces taux décrit une situation contraignante12 (c’est-à-dire une situation qui n’a pas eu lieu en réalité). Étant donné que les effets causaux sont définis comme contrastes de situations contraignantes, la raison de ces taux est un taux relatif causal.
si l’initiation de la balise avait été attribuée au hasard au début du suivi, le relatif Le taux observé serait un estimateur cohérent du taux relatif causal car les traités et non traités seraient interchangeables. En revanche, dans les études d’observation, la probabilité de recevoir le traitement s’appuie généralement sur les caractéristiques du sujet. Les patients traités ne sont généralement pas interchangeables avec ceux non traités, de sorte que le taux relatif observé ne coïncide pas avec le taux de causalité relatif13. Dans les études pharmacoépidémiologiques, ce problème est connu comme indication par indication.
Une solution au problème de la confusion est de mesurer toutes les caractéristiques des patients affectant la décision de traitement et de risque de sida / décès (par exemple, le Indications de traitement) Pour estimer le taux relatif causal chez les patients ayant les mêmes valeurs de ces variables. Cette méthode est appelée stratification. Les modèles de régression avec des covariables sont une version sophistiquée de la stratification.
Une deuxième solution au problème de la confusion consiste à mesurer les mêmes caractéristiques des patients à estimer la probabilité que chaque individu reçoive un traitement (p. Targa ou rien) qu’il a reçu en réalité. Les poids du signal sont ensuite calculés qui sont proportionnels à l’inverse de la probabilité estimée (similaire à la pondération utilisée dans certaines techniques d’échantillonnage14). La fonction des poids est de simuler une « pseudopobulation » dans laquelle chaque individu de la population d’origine est pondéré, de sorte que la répartition des caractéristiques des patients est la même parmi les traités et non traitée à chaque instant. C’est-à-dire que, en l’absence de confusion résiduelle dans la population initiale, les traités et non traités sont interchangeables dans la pseudopobulation et il n’y a pas de confusion15. Cette méthode est appelée pondération de probabilité inversée ou, dans sa forme la plus élémentaire, la normalisation. Les paramètres des modèles de structure marginaux sont estimés en pondérance par probabilité inverse8,13,16.
Les deux méthodes, la stratification et la pondération, fournissent des estateurs avec une interprétation causale uniquement sous la condition que les variables de confusion qu’elles ont été correctement mesuré. Comme il est impossible de démontrer le respect de cette condition d’absence de confusion résiduelle, des études d’observation ne peuvent pas garantir la validité causative de leurs estimateurs. Toutefois, les chercheurs peuvent augmenter la probabilité que la condition soit remplie s’ils appliquent leurs connaissances expertes et leur analyse d’étude. Par exemple, notre étude enregistre et incorpore dans l’analyse la plupart des variables d’indicateur de traitement qui sont également des facteurs de risque connus pour le sida.
Bien que la validité de la stratification et de la pondération dépend d’une condition qui ne puisse pas être vérifiée empiriquement, la pondération permet de s’ajuster correctement par les variables de confusion qui changent au fil du temps et sont affectées par le traitement précédent (par exemple, le nombre de CD4 dans notre étude). Méthodes basées sur la stratification, telles que les modèles de régression classiques (y compris le modèle COX avec des variables changeantes au fil du temps), ne permettez pas de régler correctement à ces variables de confusion, même si elles ont été correctement mesurées17. Dans cet article, nous utilisons un modèle de Cox structurel marginal pour estimer le taux relatif causal. Pour estimer les paramètres du modèle structurel marginal de COX8,13,16, un procédé divisé en 2 étapes est utilisé.
dans la première étape est estimé pour chaque sujet la probabilité de traitement de démarrage dans chaque intervalle ( Un mois, dans notre cas) en utilisant, par exemple, une régression logistique, où la variable de réponse est l’indicateur d’utilisation du traitement et les covariables sont les facteurs de risque associés au début du traitement. Chaque sujet contribue avec autant d’observations que des mois depuis le début du suivi jusqu’au début du traitement (la probabilité d’être traitée après le début du traitement est 1 sous l’hypothèse que les patients ne quittent pas Targa une fois la thérapie a été lancée).Ces probabilités sont utilisées pour estimer les poids pour chaque sujet et mois.
Dans la deuxième étape, un modèle COX est ajusté avec la variable changeant dans TARGA TIME, et aucune autre variable changeante à temps, pondérée par le temps attendu. poids à l’étape précédente. L’estimateur du taux relatif du sida / mortalité de ce modèle est un estimateur cohérent du taux relatif causal dans les conditions de spécification résiduelle et correcte de la non-confusion des modèles dans les deux étapes. Pour faciliter la programmation, approchez le modèle de COX pondéré à travers une régression logistique pondérée, dans laquelle chaque individu contribue autant d’observations que les mois de suivi. Le ratio de cotes de cette régression logistique est bien approché par le risque relatif instantané ou le taux relatif du modèle COX, car le risque d’événements (sida ou décès) était inférieur à 10% à tous les intervalles mensuels.
ci-dessous, nous présentons une description plus détaillée de ce processus en 2 étapes. Dans notre étude pour chaque observation mensuelle T de chaque individu I, un indicateur de traitement du traitement AI (T) et Li (t) covariables (CD4 et la charge virale) est disponible, qui sont utilisés pour décider de l’affectation de traitement dans le mois T . À partir de maintenant, nous éliminons l’indice I de chaque individu pour alléger la notation. Pour faire référence à l’histoire d’un dès le début du suivi jusqu’au mois, nous utilisons une barre horizontale, c’est-à-dire à (t) = {A (0), A (1) … A (t) }, et la même chose pour L. L (0) représente les mesures covariables au début du suivi (CD4, charge virale, pré-traitement, âge, sexe et temps de Seroconversion). L (0) est inclus dans l (t).
de manière informelle, le poids attribué à une personne dans le mois t est l’inverse de la probabilité que l’individu ait reçu son propre historique de traitement depuis le suivi de début du suivi. jusqu’au mois t. Ces pesos:
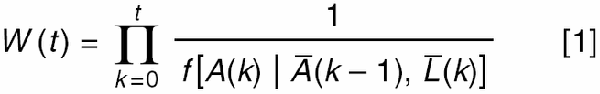
peuvent être utilisés pour ajuster par la confusion qui provoque les variables L (t). Le numérateur est, de manière informelle, la probabilité que l’individu reçoit le traitement (Targa ou rien) qu’il a réellement reçu pendant le mois k.
Cependant, les poids w (t) ont une variabilité excessive, par quoi est conseillé de les stabiliser. La stabilisation peut être réalisée en remplaçant, pour chaque mois de chaque mois, numérateur 1 pour la probabilité d’avoir reçu son propre historique de traitement à partir du début du suivi jusqu’à la période T sans conditionnement dans les variables dépendantes du temps dans L (T). Ensuite, le poids stabilisé est le suivant:

pour estimer les probabilités du numérateur de SW (t), nous ajustons le modèle de régression logistique:

où β0 (t) est modélisé, par exemple, avec une spline cubique restreinte (dans notre exemple , Avec des nœuds dans les centiles 20, 40, 60 et 80, en utilisant les valeurs par défaut de la STATI pour les pourcentages 0 et 100). Le modèle est limité aux intervalles avant le début du traitement, a (t 1) = 0, car pour le reste la probabilité de recevoir un traitement A (t) = 1 est égal à 1 sous notre hypothèse qui « une fois traitée, toujours traité « . Les probabilités estimées par ce modèle sont utilisées pour calculer la probabilité estimée à la manière dont une personne ait reçu son propre historique de traitement L (0) du début du suivi jusqu’à chaque mois.
Pour estimer les chances dans le Dénominateur, nous supposons que la décision de démarrer le traitement dans le mois T dépend uniquement de la valeur basale et de la valeur la plus récente de L, c’est-à-dire L (0) et L (t) et ajuste le modèle de régression logistique:

Nos résultats étaient similaires lorsque nous utilisons des hypothèses moins restrictives, par exemple lorsque le modèle incluait L (0) et les trois Les valeurs les plus récentes L (T), L (T 1) et L (T 2), nous avons donc décidé de présenter l’analyse la plus simple.
analogique, SWC (t) Les poids sont estimés pour ajuster pour le biais de sélection causé par une censure informative. Pour ce faire, au lieu d’estimer le poids comme une probabilité d’être traitée, le poids est estimé comme la probabilité d’être censuré. Multiplier les deux pesos, SW (T) et SWC (t), vous obtenez le poids définitif pour chaque mois de personne. Enfin, le taux de causalité relative est estimé par un modèle pondéré de Cox ou, d’une manière approximativement équivalente, à travers un modèle de régression logistique pondéré. Les estimateurs des paramètres du modèle pondéré sont des estimateurs cohérents des paramètres d’un modèle marginal structural. Une description formelle du modèle de Cox structurel marginal peut être trouvée dans les travaux de Hernan et al7.18.
Afin de comparer les résultats obtenus avec le modèle pondéré, 3 modèles logistiques non pondérés ont été ajustés.La première inclut le traitement variable au fil du temps, mais pas de covariate (modèle brut). La seconde ajoute au modèle précédéré L (0), c’est-à-dire les mesures coovariables au moment de l’entrée dans l’étude. La troisième ajoute au modèle précédent les facteurs changeants dans le temps L (T). Le modèle pondéré comprend les mêmes covariables que le deuxième modèle non pondéré. Les taux relatifs et leurs intervalles de confiance (CI) de 95% ont été estimés. Dans le modèle pondéré, la variance robuste a été utilisée pour ajuster par la corrélation induite par les poids et, par conséquent, la CI de 95% du taux relatif du modèle pondéré est conservateur (couvre plus de 95%). Les analyses ont été effectuées via le programme STATA 9.0 et pour le modèle pondéré Les instructions ont été suivies de FleLell et al19.
résultats
Le tableau 1 montre les caractéristiques des sujets admissibles de 917 qui ont été suivis pour une moyenne de 3,4 ans. 139 résultats d’intérêt (88 cas de sida et 51 décès) ont été observés, ce qui implique un taux annuel de 4,5 résultats pour 100 personnes. Pendant le suivi, 388 sujets (42,1%) ont initié Targa, ce qui implique un taux d’incidence annuel de TARGA de 21,3 pour 100 personnes; 87 des événements ont été présentés dans des personnes non traitées (incidence de 4,8%) et 52 dans des personnes traitées (incidence de 4,3%). 39,8% du temps de suivi par personne a été observé après le début de Targa. Le tableau 2 montre les facteurs associés à une probabilité plus élevée du début de Targa: sexe féminin, n’utilisez pas de médicament parentérale, intervalle à long terme du début de l’infection par le VIH et du niveau de CD4 faible dans le suivi.
logistique Les modèles de régression pour estimer le début et la censure de Targa à chaque mois ont été utilisés pour estimer les poids stabilisés. Dans la figure 1, le taux relatif (95% CI) est présenté à l’aide des différents modèles non pondérés: 1,01 (0,68-1,49) sans covariables, 0,80 (0,54-1,19) avec des mesures variables au moment initial (sexe, Traitement antirèvéral antérieur, CD4 basal, âge, temps de Seroconversion) et 0,90 (0,61-1,32) avec des mesures coovariables au moment initial et changement dans le temps (CD4). Le taux relatif causal (95% CI) estimé par le modèle pondéré avec des covariables initiaux était de 0,74 (0,49-1, 12).
dans le modèle pondéré, il n’y avait pas d’interaction significative (p = 0,522) entre le Niveau initial de CD4 et Targa. Le taux relatif causal (95% CI) était de 0,62 (0,26-1,34) pour CD4 < 200, de 0,74 (0,38-1, 43) pour CD4 200-350, de 1,24 ( 0.56-2.74) Pour CD4 350-500 et 0,57 (0,57 (0.25-1.31) pour CD4 > 500 au début du suivi.
Quand les modèles ont été ajustés dans les 437 sujets pour lesquels des mesures de charge virale étaient disponibles, les taux relatifs estimés (95% CI) étaient de 1,00 (0,68-1,49) dans le modèle non covariable, 1,02 (0,63-1,66) dans le modèle avec changement Variables au fil du temps et 0,54 (0, 24-1,26) dans le modèle pondéré.
Discussion
Études de cohorte observationnelles, telles que le projet Gemes, complétez les informations sur l’efficacité Fourni par des essais cliniques parce qu’ils reflètent mieux les conditions réelles d’application des traitements. L’utilisation des modèles structurels marginaux nous a permis d’estimer l’effet net de la balise en progression au SIDA ou à la mort après avoirjusté correctement par les facteurs déroutants dépendants du temps.
même si nos estimateurs sont plus larges que celles observé dans d’autres emplois utilisés MEM9,10, notre analyse confirme l’effet bénéfique de TARGA: une réduction de l’incidence du sida ou de la mort de 25% lorsque les poids dépendent de l’histoire individuelle du CD4 de comptage et de 46% lorsque le poids est également Dépend de l’historique des charges virales du VIH individuel. Cependant, un modèle classique (non pondéré) COX avec des variables dépendantes du temps estimé une réduction de 10% seulement. Cet effet vers la nullité est dû en partie au biais de sélection qui se produit lors de l’utilisation d’une variable comme le nombre de CD4, qui induit le traitement et, en même temps, est affecté par celui-ci17.20. Nos résultats sont compatibles avec les estimations de l’efficacité de la population obtenues par divers auteurs3-6 qui ont utilisé des méthodes basées sur la prise en compte de la période de calendrier en tant que variable instrumentale de Targa.
L’un des principaux défis de la méthode utilisée est le besoin estimer systématiquement la probabilité d’initiation de Targa dans chaque intervalle (un mois, dans notre cas). Cela nécessite d’enregistrer longitudinalement les covariables que les médecins et les patients utilisent pour décider du début du traitement.Dans le cas de l’infection à VIH, les guides de démarrage du traitement sont basés sur des charges virales et surtout dans les valeurs de CD4, qui était la variable de changement dans le temps utilisé dans notre analyse principale. D’autres facteurs pouvant être associés au début du traitement ont également été inclus dans notre analyse (sexe, catégorie de transmission, âge, temps de Seroconversion) 21. Bien que d’autres facteurs pronostiques pronostiques n’étaient pas disponibles, tels que la comorbidité ou d’autres problèmes spécifiques, nous pensons que les plus importants ont été inclus dans l’analyse.
Pour que nos estimateurs ne dépendaient pas d’hypothèses non vérifiables. En ce qui concerne notre capacité à prédire la probabilité d’abandon du traitement, nous adoptons la convention qu’une fois que le patient entre en soi traite, il en reste toujours. Le résultat de cette stratégie est que nos estimations sont analogues à celles d’un essai clinique avec une analyse de l’intention de traiter. Dans notre étude, nous ne savons pas s’il y avait des interruptions et que celles-ci étaient motivées par une mauvaise conformité thérapeutique ou par une décision clinique. Dans les études dans lesquelles ces informations sont disponibles, les modèles structurels marginaux peuvent l’utiliser pour estimer l’efficacité du traitement réel (pas l’effet par intention de traiter), à condition que la probabilité d’interruption de traitement puisse être systématiquement estimée. Il est associé au temps -Les facteurs de confusion, tels que le nombre de CD4.
Contrairement à d’autres travaux précédents99, nous n’avons trouvé aucune interaction claire du traitement avec les valeurs initiales de CD4 au début de l’étude, bien que cela puisse être en raison de différences dans la composition des cohortes. Une limitation de notre travail est que lors de la comparaison des patients traités et non traités avec Targa, ce dernier groupe comprend des traités avec une thérapie antirétrovirale non définie comme Targa. Lorsque l’analyse était limitée aux personnes qui n’avaient reçu aucun type de traitement antirétroviral au début du suivi, la réduction de l’incidence du sida ou de la mort était de 40% (taux relatif de 0,61, 95% CI, 0,30 -1, 24). Cet effet est inférieur à celui estimé précédemment dans une cohorte suisse10, mais il faut garder à l’esprit que notre analyse n’a pas pu être ajustée par la charge virale (en raison du manque de données) et que la composition de la cohorte suisse est différente de la nôtre. . Alors que la cohorte suisse est formée par des sujets séropositifs qui reçoivent des soins médicaux dans des centres hospitaliers, Gemes4 comprend certaines cohortes de Seroconverters sélectionnés en dehors de l’environnement hospitalier, dans les centres d’information sur le sida et de prévention avant 1996.
en résumé, Cet article a présenté une application du MEM au contrôle de la confusion par une indication en raison des variables changeantes d’une cohorte de patients séropositifs. Bien que les MEMS permettent d’estimer les effets causaux, même lorsqu’il existe des variables de confusion dépendantes du temps affecté par le traitement précédent, les hypothèses que ce type de modélisation nécessitent (informations fiables, aucune variables de confusion non mesurée, sans censure informative et avec une spécification correcte des modèles) ne sont pas plus restrictives que celles des méthodes conventionnelles. L’application des MEMS dans d’autres domaines de la recherche clinique et épidémiologique contribuera à évaluer les possibilités de cette méthodologie d’analyser les effets causaux sur les études d’observation.
Annexe 1. Groupe d’étude multicentrique espagnol de Serocover (Gemes)
Centre de coordination, ministère de la Santé publique, Université de Miguel Hernández: Julia del Amo, tildefonso Hernández Aguado. Centre d’analyse de données, École de santé Valencienne: Santiago Pérez-Hoyos, Ferreros Immaculée. Cohorte de l’hôpital Allemands Trias I Pujol de Badalona: Robert Muga, Arantza Sanvicens, Clotet Bonaventura, Jordi Tor. Cohort de Madrid-Sandoval: Jorge Del Romero, Paloma Raposo, Carmen Rodríguez, Soledad García, Vicente Soriano, et le groupe Seroconverters de la Communauté de Madrid. Cohorte des PIP de la Communauté valencienne: Isabel Hurtado, Manoli García de la Hera, Ignacio Alasúre, Josefina Belda, Josep Trullen, Elisa Fernández, Concha Santos, Treesa Tarif. Cohorte des centres de soins du SIDA et de prévention de Barcelone. Cohort IMSP: Patricia García de Olalla, Joan A. Caylà. Cohorte de prisons de Catalogne: Rafael Guerrero, Andrés Marco. Cohorte hémophile de la paix de l’hôpital: Manolo Quintana, Cristina González. Cohortes de l’hémophilice de l’hôpital Vall d’Hébron: Isabel Ruiz. Cohortes hémophiles de Virgen del Rocío de Sevilla: Rosario Pérez, José Miguel Cisneros. Cohorte de l’Institut de la santé publique de Navarre: Jesús Castilla.
Bibliographie
1.Hammer SM, Squires Ke, Hughes MD, Grimes JM, Demeter LM, Currier JS, et al. Un essai contrôlé de deux analogues de nucléoside plus indinavir chez les personnes atteintes d’une infection par le virus de l’immunodéficience humaine et de CD4 Compte de 200 par millimètre cube ou moins. SIDA Clinical Essais Groupe 320 Équipe d’étude. N Engl J Med. 1997; 337: 725-33.
2. Cameron Dw, Heath-Chiozzi M, Danner S, Cohen C, Kravcik S, Maurath C, et al. Essai randomisé par placebo du ritonavir dans une maladie de VIH-1 avancée. Le groupe d’étude avancé sur le ritonavir de la maladie du VIH. Lancette. 1998; 351: 543-9.
3. Donnez-vous, Muñoz A, McFarlane G, Kingsley La, Margolick JB, Giorgi J, et al. Efficacité du traitement antirétroviral puissant à temps pour le sida et la mort chez les hommes avec une durée connue de l’infection par le VIH. Les enquêteurs d’étude de cohorte multicentrique au sida. Jama. 1998; 280: 1497-503.
4. Pérez-Hoyos S, Del Amo J, Muga R, Del Romero J, García O, Guerrero R, et al. Efficacité de la thérapie antirétrovirale très active dans les cohortes espagnoles de Seroconverters VIH: Différences de la catégorie Transmission. LE SIDA. 2003; 17: 353-9.
5. Babiker A, Darbyshire J, Pezzotti P, Porter K, Rezza G, Walker Sa, et al. Changements sur le temps de calendrier dans le risque d’événements spécifiques de premier sida-définissant après la séroconversion du VIH, ajustant les risques concurrents. Int J épidémiol. 2002; 31: 951-8.
6. Porter K, Babiker A, Bhaskaran K, Darbyshire J, Pezzotti P, Walker As, et al. Déterminants de la survie après la séroconversion du VIH-1 après l’introduction de HAART. Lancette. 2003; 362: 1267-74.
7. Hernan Ma, Brumback B, Robins JM. Modèles structurels marginaux pour estimer l’effet causal de la zidovudine sur la survie des hommes séropositifs. Épidémiologie. 2000; 11: 561-70.
8. Robins JM, Hernan Ma, Brumback B. Modèles structurels marginaux et inférence causale en épidémiologie. Épidémiologie. 2000; 11: 550-60.
9. Cole Sr, Hernan Ma, Robins JM, Anastos K, Chmiel J, Dident R, et al. Effet de la thérapie antirétrovirale très active sur le temps nécessaire au syndrome de l’immunodéficience acquise ou à la mort à l’aide de modèles structurels marginaux. Je suis épidémiol. 2003; 158: 687-94.
10. Sterne Ja, Hernan Ma, Ledergerberberb B, Tilling K, Weber R, Sendi P, et al. Efficacité à long terme du traitement antirétroviral puissant dans la prévention du SIDA et de la mort: une étude de cohorte prospective. Lancette. 2005; 366: 378-84.
11. Gemes (Grupo Español MultiCéntrico Para El Esturoio de Seroconversores). El Período de Incubación del Sida en España Anties de la Terapia Antirrettroviral de Alta Eficacia. Med Clin (Barc). 2000; 115: 681-6.
12. NEYMAN J. sur l’application de la théorie des probabilités aux expériences agricoles: essai sur les principes, section 9. Science statistique. 1990; 5: 465-80.
13. Hernan Ma. Une définition de l’effet causal pour la recherche épidémiologique. J Epidemiol Santé communautaire. 2004; 58: 265-71.
14. Horvitz DG, Thompson DJ. Une généralisation de l’échantillonnage sans remplacement d’une population finie. Jasa. 1952; 47: 663-85.
15. Hernan Ma, Robins JM. Estimation des effets causaux des données épidémiologiques. J épidémiol. Santé communautaire. 2006; 60: 578-86.
16. Hernan Ma, Hernández-Díaz S, Robins JM. Une approche structurelle du biais de sélection. Épidémiologie. 2004; 15: 615-25.
17. Robins JM. Modèles structurels marginaux. Procédures ou l’American Statistical Association, section sur la science statistique bayésienne, p. 1-10. Alexandrie: Association statistique américaine; 1998.
18. Hernan Ma, Brumback B, Robins JM. Modèles structurels marginaux pour estimer l’effet de causalité conjoint des traitements non randomisés. Jasa. 2001; 96: 440-8.
19. Loupelle Z, Hernan Ma, Wolfe F, Tilling K, Choi H, Sterne Ja. Contrôle de la confusion dépendante du temps à l’aide de modèles de structure marginaux. Stata J. 2004; 4: 402-20.
20. Cole SR, Hernan Ma. La faillibilité dans l’estimation des effets directs. Int J épidémiol. 2002; 31: 163-5.
21. Ahieh L, Gange SJ, Greenblatt R, Minkoff H, Anastos K, Young M, et al. Sélection par indication d’une utilisation antirétrovirale puissante Utilisez dans une grande cohorte de femmes infectées par le virus de l’immunodéficience humaine. Je suis épidémiol. 2000; 152: 923-33.